下列说法正确的是( )
|
| A. | 相对原子质量就是原子的实际质量 |
|
| B. | 物质发生三态变化是由于分子从静止状态变为运动状态 |
|
| C. | 元素的化学性质与原子的最外层电子数没有关系 |
|
| D. | 化学反应前后原子数目没有增减 |
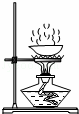
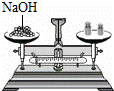
规范、正确的实验操作对实验结果、人身安全都非常重要.下列操作正确的是( )
|
| A. |
蒸发食盐水 | B. |
铁丝在氧气中燃烧 |
|
| C. |
称量NaOH固体的质量 | D. |
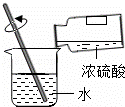
稀释浓硫酸 |
下列化学方程式书写正确的是( )
|
| A | CO2+CaCl2+H2O=CaCO3↓+2HCl | B. | NH4HCO3+HCl=NH4Cl+CO2↑+H2O |
|
|
| FeSO4+Cu=CuSO4+Fe | D. | Fe+2HNO3=Fe(NO3)2+H2↑ |
有机物在日常生活中应用广泛,下列说法正确的是( )
|
| A. | 甲烷是沼气的主要成分,沼气是可再生的生物能源 |
|
| B. | 工业酒精的主要成分是甲醇,甲醇饮后会使人失明,甚至死亡.因此,工业酒精是禁止用来配制饮用酒的 |
|
| C. | 乙酸俗称醋酸,是食醋的主要成分,纯乙酸是无色、有强烈刺激性气味的液体,且无腐蚀性,可直接食用 |
|
| D. | 合成材料主要包括塑料、橡胶和合成纤维 |
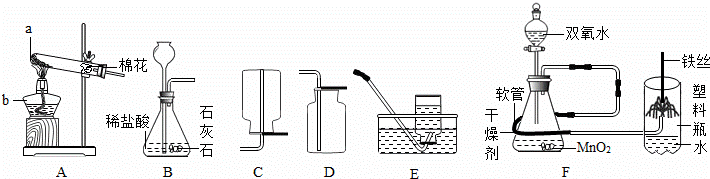
合金在生活中应用十分广泛.已知某合金粉末除含铝外,还含有铁、铜中的一种或两种.小明利用如图装置对合金粉末中铁、铜的存在进行探究时,误把氢氧化钠溶液当成稀硫酸加入到锥形瓶中,他惊奇的发现有无色气体放出,注射器活塞向右移动.
【提出问题】难道NaOH溶液也能与某些金属发生化学反应吗?
【查阅资料】
(1)铝能与氢氧化钠溶液反应,铁、铜不能与氢氧化钠溶液反应.
(2)铝与氢氧化钠溶液反应的化学方程式为:2AI+2NaOH+2H2O═2NaAIO2+3H2↑(NaAlO 溶于水,溶液现无色)
溶于水,溶液现无色)
【进行猜想】猜想1:该合金粉末中除铝外,还含有铁.
猜想2:该合金粉末中除铝外,还含有 .
猜想3:该合金粉末中除铝外,还 含有铁、铜.
含有铁、铜.
【实验探究】下列实验(见表1)仅供选用的试剂:20%的硫酸溶液、30%的NaOH溶液.
表1实验记录
| 实验步骤 | 实验现象 | 结论 |
| ①取一定量的合金粉末,加过量的 ,充分反应后过滤,滤渣备用 | 粉末部分溶解,并有无色气体放出 | 合金中一定含有 |
| ②取步骤①所得滤渣,加过量 ,充分反应 | 滤渣部分溶解,并有无色气体放出,溶液呈浅绿色 | 合金中一定含有 |
【得出结论】猜想3成立.
【反思】
1.一般来说,活泼金属能与稀硫酸等算反应,而铝与酸、碱都 能反应,说明铝具有特殊的性质.铝与稀硫酸发生化学反应的基本类型是 反应.
能反应,说明铝具有特殊的性质.铝与稀硫酸发生化学反应的基本类型是 反应.
2.上述实验中用到的稀硫酸由浓硫酸稀释得到,稀释浓硫酸的方法是:把 ,并不断搅拌.
3.若小明向合金粉末中加入的是足量的稀硫酸,则最终剩余的固体成分是 .
【拓展与分析】请你设计一个实验方案,比较铝、铁、铜的金属活动性强弱 .

在一个密闭容器中放入X、Y、Z、Q四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应认识错误的是( )
| 物质 | X | Y | Z | Q |
| 反应前质量(g) | 20 | 2 | 1 | 37 |
| 反应后质量(g) | 未测 | 32 | 1 | 12 |
|
| A. | 物质Z可能是该反应的催化剂 | B. | 反应后物质X的质量为15g |
|
| C. | 反应中Y、Q的质量比为6:5 | D. | 物质Y一定是单质 |
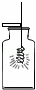
 .
. C.
C.