右图为元素周期表第三周期的局部。据此判断下列说法中正确的是:
A、硅元素的原子序数为14
| 11Na 23.00 | 12Ma 24.31 | 13Al 26.98 | 14Si 28.09 |
B、镁元素的相对原子质量为12
C、1个铝原子的质量是26.98g
D、它们都属于金属元素
猪血中含有卟啉铁(C34H32C1FeN4O4)对缺铁性贫血有显著效果。以下说法不正确的是
A、卟啉铁中含有6种元素 B、干净的猪血是化合物
C、卟啉铁中碳元素的质量分数最大 D、人体补铁还有其他方法
铝制 品不宜长时间盛放腌制食品。资料显示:“铝制品表面虽然有一层致密的氧化膜保护……氯化钠也会破坏氧化膜的结构,加速铝制品的腐蚀。”
品不宜长时间盛放腌制食品。资料显示:“铝制品表面虽然有一层致密的氧化膜保护……氯化钠也会破坏氧化膜的结构,加速铝制品的腐蚀。”
【提出问题】氯 化钠溶液中的哪一种离子对铝制品表面的氧化膜产生了破坏作用?
化钠溶液中的哪一种离子对铝制品表面的氧化膜产生了破坏作用?
【猜 想】
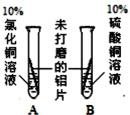
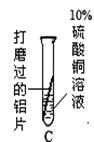
【实验方案】请填写下面表格中的空格。
| 序号 | 实验1 | 实验2 | 实验3 |
| 方 案 |
|
|
|
| 现 象 | A中铝片 B中铝片无明显现象。 |
| 与A中的现象相同 |
| 结 论 | 溶液中对氧化膜产生了破坏作用的离子可能是 。 | 除去表面氧化膜的铝片会与CuSO4溶液反应。该反应 的化学方程式 。 | 验证了实验1的结论。 |
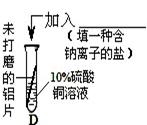
【反思】针对实验3,同学认为还应增做一个对比实验,方案是向 (从“A、B、C、D”中选择)试管中再加入Na2SO4溶液,结果无明显现象。该实验可证明溶液中对氧化膜不产
(从“A、B、C、D”中选择)试管中再加入Na2SO4溶液,结果无明显现象。该实验可证明溶液中对氧化膜不产 生破坏作用的离子是 。
生破坏作用的离子是 。
实验室常用的干燥剂“碱石灰”是CaO和NaOH固体的混合物,极易与空气中水蒸气和CO2反应而变质。同学们为确认一瓶久置的“碱石灰”样品的成分,进行如下实验探究 。
。
(1)【猜想】猜想Ⅰ:没有变质,“碱 石灰”中只含有CaO、固体NaOH;
石灰”中只含有CaO、固体NaOH;
猜想Ⅱ:已完全变质,“碱石灰”全部变成了CaCO3和 Na2CO3
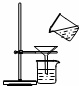
(2)【 实验】如图所示:
实验】如图所示:
|
|

实验过程中,同学们还发现向样品中加入足量水溶解时放出大量的热。
( 3)【判断】
3)【判断】
a.若Ca(OH)2、CaCO3和Na2CO3溶于水无明显的温度变化,则猜想Ⅱ______________ ;
;
(填“成立”或“不成立”)
b.操作④发生反应的化学方程式为______________________________________;
由操作③的现象判断:滤渣一定含有_______________(写化学式);
由此判断猜想Ⅰ_________(填“成立”或“不成立 ”)
”)
c.综合a和b的结论,判断该样品变质情况为_______(填“全部变质”或“部分变质”)
下列对样品成分的分析正确的是_____(填序号)。
① 样品中一定含NaOH ② 样品中一定含Na2CO3
③ 样品中含NaOH、CaO中的一种或两种
【拓展】由上述实验说明,实验室中“碱石灰”应_ __保存;操作②中玻璃棒的作用是_____。
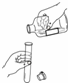

 表面有红色固体析出;
表面有红色固体析出;