为了确保食品安全,下列物质在生产、生活中的用途合理的是( )
|
| A. | 用大量的亚硝酸钠腌制食品 | B. | 用碳酸氢钠焙制糕点 |
|
| C. | 用甲醛溶液浸泡海产品 | D. | 用“塑化剂”制饮料 |
日常生活中的下列变化,其中一种变化与其余三种变化类型不同的是( )
|
| A. | 酒精挥发 | B. | 铁棒磨成针 | C. | 食品腐烂 | D. | 花香四溢 |
某实验小组利用废硫酸液制备K2SO4并研究CaSO4•2H2O加热分解的产物。
 一、K2SO4的制备
一、K2SO4的制备
(1)将CaCO3研成粉末的目的是 ▲ 。
(2)上述流程中可循环使用的物质有CO2和 ▲ (填写化学式)。
(3)反应Ⅲ中相关物质的溶解度如下表。你认为反应Ⅲ在常温下能实现的原因是 ▲ 。
| 物质 | KCl | K2SO4 | NH4Cl | M |
| 溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
(4)不用水而用饱和K2SO4溶液洗涤反应Ⅲ所得晶体的目的是 ▲ ;为检验此晶体是否洗涤干净,可取最后 一次洗涤液,先加入 ▲ (选填序号,下同),振荡、静置,再向上层清液中滴加 ▲ ,观察现象即可判断。
一次洗涤液,先加入 ▲ (选填序号,下同),振荡、静置,再向上层清液中滴加 ▲ ,观察现象即可判断。
a.AgNO3溶液 b.过量的BaCl2溶液 c.过量的Ba(NO3)2溶液
(5)分离所得的CaSO4•2H2O含有CaCO3,可用盐酸除去,该的化学反应方程式 ▲ 。
 (6)为了测定CaSO4•2H2O和CaCO3的质量比x:y,实验小组利用下图所示的装置(夹持仪器省略)进行实验。
(6)为了测定CaSO4•2H2O和CaCO3的质量比x:y,实验小组利用下图所示的装置(夹持仪器省略)进行实验。

 |
|
①实验前首先要 ▲ ,再装入样品。装置A的作用是 ▲ 。
②已知CaSO4•2H2O在160℃生成CaSO4,1350℃时CaSO4开始分解;CaCO3在900℃时分解完全。现控制B装置温度900℃进行实验并采集了如下数据:
a.反应前玻璃管与样品的质量m1g b.反应后玻璃管中固体的质量为m2g
c.装置C实验后增重m3g d.装置D实验后增重m4g

 某同学选用b、d或c、d数据组合求出x:y的值,若无装置E,则实验测定结果将 ▲ (填“偏大”、“偏小”或“无影响”)。你认为还可选用上述的 ▲
某同学选用b、d或c、d数据组合求出x:y的值,若无装置E,则实验测定结果将 ▲ (填“偏大”、“偏小”或“无影响”)。你认为还可选用上述的 ▲  (选填序号)两个数据组合也可求出x:y的值。
(选填序号)两个数据组合也可求出x:y的值。
(7)CaSO4•2H2O受热会逐步失去结晶水。取纯
净CaSO4•2H2O固体3.44g,放在(5)的实
验装置B中进行加热,测定固体质量随温
度的变化情况如右图所示。
①G点固体的化学式是 ▲ 。
②将T2~1400℃温度段加热固体所产 生的
生的
气体
|
则H~I段发生反应的化学方程式为 ▲ 。
 下图表示某些物质间转化关系。A、D为固体且组成元素相同,A为紫黑色;X、F为液体且组成元素相同,X具有消毒杀菌作用;E为产生温室效应的常见气体,Y是一种红色的金属。请回答下列问题:
下图表示某些物质间转化关系。A、D为固体且组成元素相同,A为紫黑色;X、F为液体且组成元素相同,X具有消毒杀菌作用;E为产生温室效应的常见气体,Y是一种红色的金属。请回答下列问题:

(1)D的化学式 ▲ ,F的化学式 ▲ ;
(2 )写出有关反应的化学方程式:② ▲ ;⑤ ▲ 。
)写出有关反应的化学方程式:② ▲ ;⑤ ▲ 。
 (3)反应⑥在催化反应室中进行,且发生多个反应,请推断完成反应(4)的化学方程式:
(3)反应⑥在催化反应室中进行,且发生多个反应,请推断完成反应(4)的化学方程式:
 |
(1)CH4+2H2O CO2+4H2 (2)CH4 C+2H2

 (3)C+CO2 2CO (4)CH4+ +3H2
(3)C+CO2 2CO (4)CH4+ +3H2
(4)利用合成气在一定条件下可合成化工产品乙醇(C2H6O),请写出该化学反应方程
式 ▲ ; 结合反应②⑥,可看出CH4不仅可作燃料,而且是重要的 ▲ 原料。
|
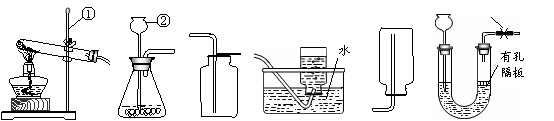 请结合下图回答问题:
请结合下图回答问题:
 |
|
|
(1)标号①②的仪器名称:① ▲ ,② ▲ 。
(2)实验室 选用A、D装置制取O2,气体收集完毕时,应先 ▲ (填“从水
选用A、D装置制取O2,气体收集完毕时,应先 ▲ (填“从水 中取出导气管”或“熄灭酒精灯”)。
中取出导气管”或“熄灭酒精灯”)。
(3)实验室可用(NH4)2SO4固体和熟石灰混合加热制取NH3,应选择发生装置为 ▲ (选
填序号)。
 (4)选择发生装置B和收
(4)选择发生装置B和收 集装置 ▲ (选填序号)可以用于实验室制取CO2,若将发生装置由B改为F,其优点是 ▲ 。
集装置 ▲ (选填序号)可以用于实验室制取CO2,若将发生装置由B改为F,其优点是 ▲ 。
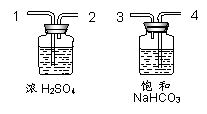
①为了得到纯净、干燥的CO2,除杂装置(如右图)
的导管按气流方向连接顺序是 ▲ (选填字母);
a.1→2→4→3 b.2→1→3→4
c.4→3→1→2 d.3→4→2→1
用化学反应方程式表示饱和NaHCO3溶液的作 用 ▲ 。
用 ▲ 。
②写出用澄清石灰水检验CO2的化学反应方程式 ▲ 。
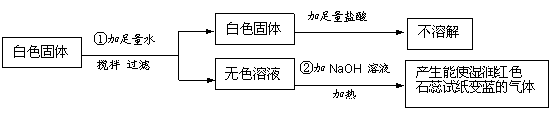 有一包白色固体粉末,可能含有CuSO4、Na2SO4、(NH4)2CO3、BaCl2、NH4Cl 、KCl中的一种或几种。现做如下实验:
有一包白色固体粉末,可能含有CuSO4、Na2SO4、(NH4)2CO3、BaCl2、NH4Cl 、KCl中的一种或几种。现做如下实验: