过碳酸钠(2Na2CO3·3H2O2)广泛用于洗涤、纺织、医疗、造纸等。某兴趣小组展开了深入的学习:
【资料卡片】:
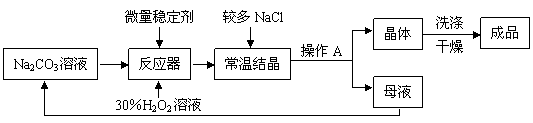
Ⅰ、制备研究:下图是制备过碳酸钠的工艺流程。
 |
请回答问题:
(1)反应器中发生反应的化学方程式为 ▲ ;
(2)生产中,反应及干燥均需在较低温度下进行,原因是 ▲ ;
(3)生产过程中,需加入较多的NaCl,以便过碳酸钠晶体析出,这是因为 ▲ 。
(4)操作A的名称是 ▲ ,若在实验室完成此操作,需要的玻璃仪器是烧杯、 ▲
和 ▲ ;
(5)洗涤过碳酸钠晶体最好选用 ▲ 。
A.蒸馏水 B.无水酒精 C.饱和碳酸钠溶液 D.饱和NaCl溶液
(6)母液可以循环使用,其中主要含有的溶质是 ▲ 和 ▲ ;
Ⅱ、纯度测定:测定过碳酸钠样品(杂质不溶于水)中2Na2CO3·3H2O2的质量分数。
小组同学设计了如下图所示实验装置(部分仪器略去),并进行实验。
 【实验步骤】:① ▲ ;②将过碳酸钠样品(2.20g)和少许黑色粉末均匀混合后置于装置A中,在量筒中加满水;③连接仪器,打开分液漏斗活塞,缓缓滴入水;④待装置A中 ▲ 时,停止滴加水,并
【实验步骤】:① ▲ ;②将过碳酸钠样品(2.20g)和少许黑色粉末均匀混合后置于装置A中,在量筒中加满水;③连接仪器,打开分液漏斗活塞,缓缓滴入水;④待装置A中 ▲ 时,停止滴加水,并 关闭活塞;⑤待量筒中水面不再变化时,记录其中水面刻度;⑥根据数据进行计算。
关闭活塞;⑤待量筒中水面不再变化时,记录其中水面刻度;⑥根据数据进行计算。
【实验分析及数据处理】:
(7)完善实验步骤的相关内容:① ▲ 、④ ▲ ;
(8)实验中,水的作用是 ▲ ;黑色粉末能加快过碳酸钠的分解速率,其自身质量和化学性质在反应前后均不变,可能是 ▲ (填化学式);
(9)实验中, ▲ ,则开始收集气体;(2分)
A.刚开始出现气泡时 B.当气泡均匀连续出现时
C.若用带火星木条放在导管口部,复燃时
(10)若量筒中收集到气体的体积是224mL(通常情况下,氧气的密度近似为1.43g·L—1。),计算过碳酸钠样品中2Na2CO3·3H2O2的质量分数[3分,Mr(2Na2CO3·3H2O2)=314、Mr(O2)=32] ▲ ;
【实验反思】:
(11)经过讨论,小组同学一致认为测定结果偏大,可能原因是 ▲ ;
(12)量筒中长导管的作用是 ▲ ;
(13)有同学提出,装置中原有空气会使测定结果偏大。这种说法是否正确,如不正确,请说明理由。 ▲ ;
(14)经过讨论,小组同学一致认 为可用下述方案进行测定。方案:将装置A中剩余物过滤,洗涤滤渣,并将洗涤液并入滤液蒸发得无水固体1.39g。则样品中2Na2CO3·3H2O2的质量分数为 ▲ 。
为可用下述方案进行测定。方案:将装置A中剩余物过滤,洗涤滤渣,并将洗涤液并入滤液蒸发得无水固体1.39g。则样品中2Na2CO3·3H2O2的质量分数为 ▲ 。
(15)根据资料卡片,你还能设计出什么方案测定样品中2 Na2CO3·3H2O2的质量分数? ▲ 。(只需给出简要的方案)
Na2CO3·3H2O2的质量分数? ▲ 。(只需给出简要的方案)
关注碳排放。
(1)化石燃料属于 ▲ (填“可再生”或“不可再生”)能源,请你推荐一种新型绿色的能源 ▲ ;
(2)下列做法不符合“低碳”生活理念的是 ▲ ;
A.使用一次性木筷和纸巾 B.推广电热水器 C.逐步淘汰白炽灯
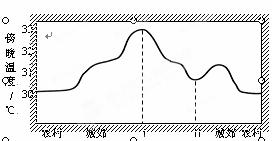
(3)CO2过多排放是城市“热岛效应”的原因之一。右图中地点Ⅰ、Ⅱ分别为
▲ ;
A.农田、商业区
B.公园、居民区
C.市中心、公园
(4)下表是CO2排放系数及一个家庭的月消耗(产生)数量:
| 项目 | 电 | 液化石油气 | 自来水 | 垃圾 | …… |
| 系数 | 0.36 kg/kwh | 6.3 kg/m3 | 0.58 kg/m3 | 0.84 kg/ kg | …… |
| 数量(/月) | 100 kwh | 7 m3 | 5 m3 | 15 kg | …… |
则一个家庭每月至少排放 ▲ kg CO2;
 (5)研究发现:CO2和H2在催化剂、加热条件下反应生成甲醇(CH4O)和水,反应的化学方程式为 ▲ 。金属铈(Ce)和CO2、H2O在900℃条件下反应,生成两种可燃性气体和CeO2,反应的化学方程式为 ▲ 。利用CO2和环氧乙烷制成的塑料无污染、易降解,可减少 ▲ 的发生。
(5)研究发现:CO2和H2在催化剂、加热条件下反应生成甲醇(CH4O)和水,反应的化学方程式为 ▲ 。金属铈(Ce)和CO2、H2O在900℃条件下反应,生成两种可燃性气体和CeO2,反应的化学方程式为 ▲ 。利用CO2和环氧乙烷制成的塑料无污染、易降解,可减少 ▲ 的发生。
材料在生活中应用很广泛。
(1)下列生活物品属于无机材料的是 ▲ ;
 |
A.玻璃杯 B.铁锅 C.塑料桶 D.玻璃钢转椅
(2)现行流通的硬币材质均为金属材料,如一元硬币是钢芯镀镍(Ni),伍角硬币是钢芯镀铜,一角硬币是铝合金或不锈钢。
①选择铸造硬币的材料不需要考虑的因素是 ▲ (填序号);
A.金属的导电性 B.金属的耐腐蚀性
C.金属的硬度 D.金属价格与硬币面值的吻合度
②五角硬币镀铜是因为常温下,铜的化学性质 ▲ (填“稳定”或“活泼”);
③钢是一种含碳量为 ▲ (填数值)的铁合金,其硬度比铁 ▲ (填“大”或“小”);
④在一定条件下,镍在空气中会形成致密的氧化膜(NiO),反应的化学方程式为 ▲ 。镍和稀硫酸反应会生成硫酸镍(NiSO4)和一种可燃性气体单质,反应化学方程式为 ▲ ;
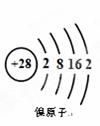
⑤根据右图镍原子的结构示意图回答:镍原子的原子序数是 ▲ ,在化学变化中易 ▲ 电子(填“得到”或“失去”)。
某钢铁厂用8 00吨(Fe%=75%)FeO、Fe2O3、Fe3O4的混合铁矿石炼铁,炼得生铁(非铁元素含量<8%)的质量可能是(生铁中C%为2% ~ 4.3%)
00吨(Fe%=75%)FeO、Fe2O3、Fe3O4的混合铁矿石炼铁,炼得生铁(非铁元素含量<8%)的质量可能是(生铁中C%为2% ~ 4.3%)
| A.600吨 | B.608吨 | C.625吨 | D.676.5吨 |
下列物质的除杂实验中,所选用的试剂、方法及反应类型均正确的是
| 选项 | 物质(括号内为杂质) | 试剂、方法 | 反应类型 |
| A. | CaO(CaCO3) | 高温 | 分解反应 |
| B. | Fe(Fe2O3) | 足量CO | 置换反应 |
| C. | CO2(CO) | 足量O2 | 化合反应 |
| D. | CaCl2溶液(HCl) | 足量CaCO3 | 复分解反应 |
右图是甲、乙两种固体的溶解度曲线,下列说法正确的是
| A.甲的溶解度大 |
| B.10℃时,等质量的甲乙饱和溶液中溶质质量相等 |
| C.20℃时,将10g甲物质加入50g水中,得到60g溶液 |
| D.30℃时,甲物质饱和溶液中,溶质质量分数最大为60% |