在去年的实验操作及理论考试中,小林同学抽签选中的两道考题是:
考题Ⅰ:用给定的碳酸钠溶液鉴别稀盐酸、食盐水和澄清石灰水;
小林同学按以下过程进行作答:
【进行实验】
| 操作步骤 | 实验现象 | 实验结论 |
| 分别用A、B、C三支试管取样,然后各加入适量碳酸钠溶液 | A中无明显现象 B中 ▲ C中 ▲ | A中物质是食盐水 B中物质是稀盐酸 C中物质是澄清石灰水 |
【发现问题】如何 处理上述废液才能减少对环境的污染?
处理上述废液才能减少对环境的污染?
【思考与分析】应先对废液中的溶质成分进行探究,后制定方案。
【实验与探究】
(1)小林将所有废液倒入一洁净烧杯中,静置后得到上层清液。
(2)取少量清液加入适量的氯化钙溶液(中性),再滴加几滴无色酚酞试液,若出现
▲ 的现象,说明上层清液中一定有碳酸钠和氢氧化钠,一定没有 ▲ 。(填离子符号)
【方法与应用】通过以上探究,处理上述废液的正确方法是 ▲ 。
考题Ⅱ:自选一种试剂鉴别氢氧化钠、氯化钠和硝酸铵三种白色固体。
小林选择出了一种试剂,通过实验并观察现象,很快鉴别出了上述三种物质,该试剂是
▲ ,小林应观测的现象是 ▲ 。实验验完成后,小林将上述物质倒入实验室废液缸中,立刻闻到一股强烈的氨味,其原因是 ▲ 。
溶液的应用非常广泛K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如下:
| 温度/℃ | 20 | 30 | 50 | 60 | 80 | |
| 溶解度/g | K2CO3 | 110 | 114 | 121 | 126 | 139 |
| KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 |
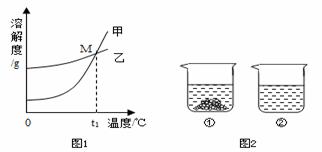
(1)图1中能表示KNO3溶解曲线的是 ▲ (填“甲”或“乙”)
⑵曲线上M点的含义是 ▲ 。
⑶40℃时,向两个分别盛有相同质量的硝酸钾和碳酸钾的烧杯中,各加入100g水,充分溶解后,恢复至40℃,其结果如图2所示。
下列有关说法中,正确的有 ▲ 。(填字母)
A.烧杯①中溶解的是KNO3,烧杯②中溶解的是K2CO3
B.烧杯②中溶液是不饱和溶液
C.升高温度或增加溶剂都有可能将烧杯①中固体全部溶解
D.若将烧杯①中的溶液变为不饱和溶液,溶液中溶质质量分数一定减小
E.将得到的烧杯②中溶液降温至20℃时,溶液中溶质质量分数可能不变
2013年3月22日是第二十一届“世界水日”。 今年的主题是“水合作”。水与人类的生活和生产密切相关,国家新版《生活饮用水卫生标准》从今年7月1日起强制实施,下表是我国颁布的生活饮用水水质标准 的部分内容。
的部分内容。
| 项目 | 标准 |
| 感官指标 | 无异味、异臭等 |
| 化学指标 | pH 6.5~8.5,铜<1.0mg•L-1,氟化物<1.0mg•L-1,游离氯≥0.3mg•L-1等 |
⑴感官指标表现的是自来水的 ▲ 性质(填“物理”或“化学”);若化学指标中的 pH=8时,表明自来水呈 ▲ (填“酸性”、“碱性”或“中性”)。
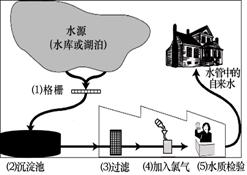
右图表示某市饮用水的净化过程,请回答下列问题:
⑵天然水中含有许多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化,其中净化程度最高的方法是
▲ 。
⑶硬水给生活和生产带来很多麻烦,生活中可用 ▲ 来区分硬水和软水,常用 ▲ 的方法来降低水的硬度。
⑷用液氯消毒杀菌的过程中,水中残留的游离氯有少量可转变成氯离子,氯离子的符号是
▲ 。
⑸饮用水消毒剂除了目前采用的液氯以外,补充了氯胺(NH2Cl)、臭氧(O3)等。O3中氧元素的化合价是 ▲ 。NH2Cl中氯元素与氢元素的质量比是 ▲ 。
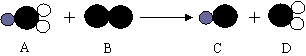 ⑹ClO2是新一代饮用水的消毒剂,可以用来代替Cl2进行自来水的消毒。制取ClO2的反应过程示意图如下:
⑹ClO2是新一代饮用水的消毒剂,可以用来代替Cl2进行自来水的消毒。制取ClO2的反应过程示意图如下:
 (其中, 表示钠原子, 表示氯原子, 表示氧原子)
(其中, 表示钠原子, 表示氯原子, 表示氧原子)
该反应的化学方程式是 ▲ 。
下表物质符合图中转化关系的是
| 选 项 |
| 乙 | 丙 | 转化关系图 |
| A | C | CO2 | CO |
|
| B | CaCO3 | Ca(OH)2 | CaCl2 | |
| C | CuO | H2O | O2 | |
| D | NaCl | NaNO3 | NaOH |

 色固体,E俗称小苏打。图中“—”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质。(部分反应物、生成物及反应条件略去)。回答下列问题:
色固体,E俗称小苏打。图中“—”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质。(部分反应物、生成物及反应条件略去)。回答下列问题:
 镀液进行了探究。
镀液进行了探究。
 到的水的体积总是比理论值
到的水的体积总是比理论值
 甲
甲