对比学习有利于发现事物的共性与个性。为探究酸的性质,同学们进行了如下实验。
| 实验内容 | 实验现象 | 分析与结论 | ||||||||||||||
|
 
| A试管内(29) ,B试管中镁带表面冒气泡。 | 酸的很多反应通常在水溶液中才能完成。 | ||||||||||||||
|
 
|
(30) (填“浓”或“稀”)盐酸瓶口的蓝色石蕊试纸很快变红。 | 即使是同种酸,由于 (31) 不同,它们的性质不完全相同。 | ||||||||||||||
|

| 两试管中均产生(32) | 不同的酸具 | ||||||||||||||
|
 
| E试管中产生(34) , F试管中无明显现象。 | 不同的酸根会导致酸的“个性”差异。因此,可用氯化钡溶液鉴别盐酸和硫酸。 |
清洗试管时,小乔同学将C、F两试管中的无色液体同时倒入一个洁净的废液缸,废液缸中立刻冒气泡并出现白色沉淀。请分析上述现象并回答:
Ⅰ. 废液缸中产生气体的反应的化学方程式为(35) 。
Ⅱ. 废液缸里最终产生的白色沉淀中一定有硫酸钡,可能有(36) (填化学式)。
课外活动时,同学们采用以下两种方法测定某氯化钠溶液的溶质质量分数。
【化学方法】向一定量氯化钠溶液中加入足量硝酸银溶液,得到0.02mol氯化银固体,则该氯化钠溶液中氯化钠的质量为(26) g(根据化学方程式列式计算)。
经多次实验测定,该溶液的溶质质量分数为10%。
【物理方法】取一定量该溶液进行蒸发,测量实验数据如下:
| 蒸发皿的质量(g) | 25.0g |
| 蒸发皿+食盐溶液(g) | 45.0g |
| 蒸发皿+食盐晶体(g) | 27.4g |
| 数据处理 | 溶液的溶质质量分数为 ( |
若化学方法测定结果准确,则物理方法测定结果产生误差的原因是(28)
A.蒸发时未用玻璃棒搅拌 B.所取氯化钠溶液质量较大
C.蒸发时出现少量晶体时就停止加热 D.实验后未将玻璃棒上的白色固体移入蒸发皿
KNO3和NaCl是日常生产生活中常见的两种盐。
① 在农业生产中,(5)是种常见的复合肥。
② 食盐是最常用的调味品。炒菜时不小心将食盐洒在火焰上,可观察到火焰呈(6)色。
③ 下表是KNO3和NaCl的溶解度。
|
I.0℃时,KNO3的溶解度是(7) g/100g水。
II.“海水晒盐”是获得食盐晶体(粗盐)的主要方法,选择这种结晶方法的依据是(8) 。
III.在不改变溶液浓度的条件下,将接近饱和的KNO3溶液变为饱和所采用的方法是(9) 。
IV.当温度在(10)(填相邻温度范围)时,能够配制浓度相等的KNO3和NaCl的饱和溶液。





 有相似的性质,这是因为酸的组成中都含有(33) (填元素符号)。
有相似的性质,这是因为酸的组成中都含有(33) (填元素符号)。
 27)
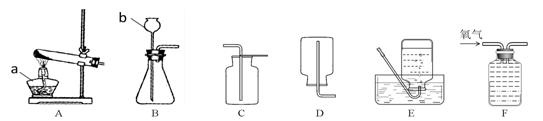
27) 
 Cu+FeSO4 ,该反应利用了铁的金属活动性比铜(14) (填“强”或“弱”)。
Cu+FeSO4 ,该反应利用了铁的金属活动性比铜(14) (填“强”或“弱”)。