如图A所示是用白磷(着火点为40℃)验证质量守恒定律的装置,其中细玻璃管的底端刚好与白磷接触。
| 实验步骤 | 现象 |
| 将装置A放在 (8) (填仪器名称)上称量。 | 示数为158.4 g。 |
| 取下带有细玻璃管的橡皮塞,用酒精灯加热细玻璃管下端至红热,迅速塞紧锥形瓶并引燃白磷。 | 白磷燃烧,产生大量 (9) ,并放出热量,气球膨胀。 |
| 冷却至室温如图B所示,再次称量装置 | 气球变瘪,质量为158.4 g |
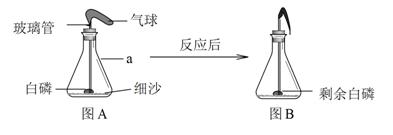
① 仪器a的名称是(10)
② 白磷燃烧的化学方程式是(11),由上述实验知,剩余气体的化学性质是(12) 。
用具体的反应物和生成物分析两次称量质量不变的原因(13) 。
③ 另一名同学在其实验结束后发现第二次称量的质量减小了,可能的原因是(14) 。
Ⅰ.白磷的量不足 Ⅱ.白磷过量 Ⅲ.反应中气球膨胀了 Ⅳ.装置密闭性不好
④ 反应结束时(如图B所示),气球变瘪的原因是(15) 。
⑤ 拓展实验:应用质量守恒定律验证石墨的元素组成。
实验步骤:称量m1 g石墨;放入盛有足量氧气的密闭容器中引燃;反应结束后,用足量的m2 g石灰水吸收生成的气体(吸收完全);称量石灰水的质量变为m3 g;
数据分析:根据(16) 可知石墨中含有碳元素;根据(17) 可知石墨中只含有碳元素。
某班级同学对实验室制取二氧化碳的若干问题进行如下探究
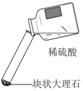
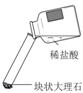
【实验一】:实验室制取二氧化碳的原料的选择,实验内容和现象记录如下
| 实验 |
|
|
|
| 现象 | 剧烈反应,产生大量气泡,反应迅速停止 | 产生气泡,速率迅速减慢,反应几乎停止。 | 产生气泡,反应持续时间较长 |
| 分析 | 反应速率过快,气体不便收集 | 无法持续产生CO2 | (1) |
| 结论 | 实验室制取二氧化碳的原料是 (2) 。 |
【实验二】:设计实验发生装置和收集装置
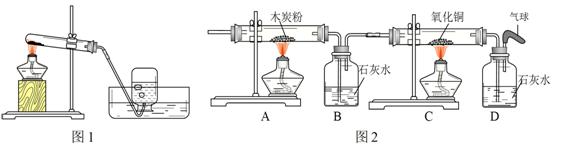
① 如图1所示是制取和收集二氧化碳的装置,其中气体发生装置的适用范围是(3) ,集气瓶中导管应处的位置是(4) (填“a”或“b”)。
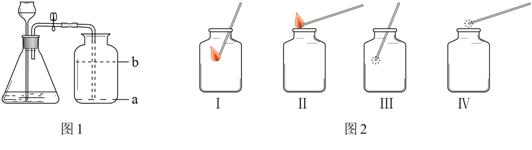
② 图二中,能够检验二氧化碳是否收集满的方法是 (5) 。
③ 该发生装置不具有启普发生装置的原理,理由是(6)
Ⅰ. 不能控制反应的Ⅱ. 不能控制反应的停止
Ⅲ .不能控制反应的发生和停止
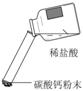
【实验三】计算实验室使用的大理石中碳酸钙的质量分数
用足量的盐酸与12 g块状大理石反应,得到0.1mol二氧化碳(杂质不参加反应)。
④ 求块状大理石中碳酸钙的质量。(请根据化学方程式计算)
⑤ 该大理石中碳酸钙的质量分数是(7) (精确到0.1%)。
硝酸钾和氯化钠的溶解度曲线如图所示,请回答:
① 10℃时,硝酸钾的溶解度是(13) g/100g水。
② 20℃时,饱和溶液的溶质质量分数比较大的是(14) 。
③ 10℃时,向50 g水中加入x g硝酸钾,可以形成饱和溶液,则x应为(15) 。
| ④ 工业上将硝酸钾和氯化钠的热混合溶液(两者均己达到饱和)冷却至室温.析出晶体中的主要物质是(16),下列关于剩余溶液的说法正确的是(17) 。 |
|
今年是“国际化学年”,化学帮助我们从认识身边的物质开始认识世界。
① 空气与我们密不可分,其中含量最多的物质是 (1) (填化学式)。二氧化硫排放到空气中引起的环境问题是(2) ,化学研究者建议用碱性物质吸收二氧化硫以减少其排放。
② 二氧化碳被认为是温室效应的元凶之一,目前科学家正致力于研究海洋封存二氧化碳,其
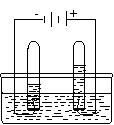
| 中一个办法是将其固体沉入海底。二氧化碳固体俗称(3)。 ③ 水被称为生命之源,右图实验能确定水的元素组成,a试管中的气体是(4) 。 ④ 醋酸是生活中的常用物质,不仅可做调味剂,也可用于除去水垢。醋酸(C2H4O2)由(5)种元素组成,各元素的原子个数比是(6),0.5mol C2H4O2中约含有(7)个氢原子。 |
 |
|
|
A、甲一定是一氧化碳 B、乙一定不是二氧化碳
C、丙可能是碳或二氧化碳 D、丁可能是碳或氧气