下表是KNO3、NaCl在不同温度下的溶解度表(单位:g/100g水)
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| KNO3 | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | 246 |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
①请写出表中“20.9”的意义是(20) 。
②40℃时,50g水溶解 (21) g KNO3形成饱和溶液,若将该饱和溶液冷却到20℃时,析出KNO3晶体 (22) g。
③通过表内数据,可知在某一温度下KNO3和NaCl的溶解度相等,该温度约为(23) ℃。
(填写温度范围的不给分)
④某硝酸钾饱和溶液的溶质质量分数为24%,则该溶液的温度是 (24) ℃。
⑤物质的溶解度往往还用“溶解度曲线图”来表示,与“溶解度表”相比较,你认为哪个更好,理由是(25) 。
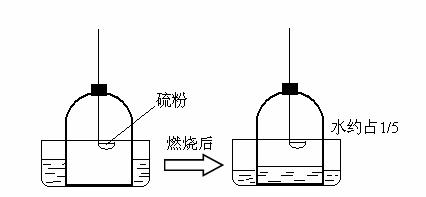 ③实验室常用白磷燃烧来验证空气中氧气约占1/5,小张同学利用实验室现有的药品硫粉和镁粉,利用下列钟罩装置进行实验,燃烧完毕冷却后的结果如图:
③实验室常用白磷燃烧来验证空气中氧气约占1/5,小张同学利用实验室现有的药品硫粉和镁粉,利用下列钟罩装置进行实验,燃烧完毕冷却后的结果如图: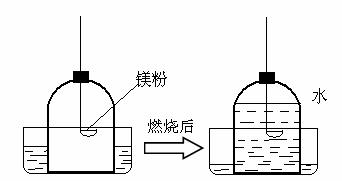
 其中发生化学变化的步骤是 (15) (填写步骤序号),
其中发生化学变化的步骤是 (15) (填写步骤序号),