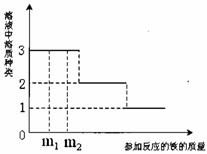
初三(2)班同学在实验室进行三种碳酸盐(碳酸氢铵、碱式碳酸铜、碳酸钙)的性质对比实验。
(1)下面是同学实验的现场实录,请根据现象判断失误原因,并将对应选项填在下面的表格。
| 操作 | 操作上的失误 |
| 小余同学加碱式碳酸铜粉末时将其沾在试管口及内壁上 | |
| 小李同实验学桌上滴瓶里的酚酞试液变红了 | |
| 小青同学在装有碳酸氢铵的试管内加入稀盐酸时,气泡带着泡沫冲出了试管 | |
| 小敏同学在测定碳酸钙上层清液pH值时,发现测定值偏小 | |
| 小帆同学用刚测完碳酸氢铵溶液pH的玻璃棒直接伸入碱式碳酸铜的上层清液,测其pH |
★失误选项:A 没有逐滴滴加稀盐酸 B 玻璃棒没有洗净擦干
C 没有将粉末状药品送入试管底部,再将试管直立起来 D 加入药品太多
E 测定溶液pH值时,先将试纸润湿再蘸取待测液于pH试纸上
F 用滴瓶上的滴管取用氢氧化钠溶液
(2)加热烧杯时应 (“直接”或“间接”)加热,水浴加热的特点是
(3)通过本实验和你已学过的化学知识,你认为
①本实验中三种碳酸盐热稳定性由强到弱的顺序是:
②酸的溶液 (填“一定”或“不一定”,下同)呈酸性,碱的溶液 呈碱性,盐的溶液 呈中性。
(4)请分别写出碳酸氢铵、碱式碳酸铜和稀盐酸反应的化学方程式:
;
。
下图装置可以完成多个简单实验,具有药品用量
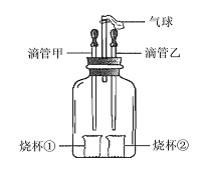 少、实验现象明显、尾气不处逸等优点。
少、实验现象明显、尾气不处逸等优点。
⑴若甲中吸有浓氨水,乙中吸有无色酚酞溶液,将甲、
乙中的液体同时挤出,一段时间后,观察到无色酚
酞溶液变红,说明分子具有的性质是 。
⑵ 若甲中吸有水,乙中吸有稀硫酸,烧杯①中盛有用
石蕊溶液染成紫色的干燥纸花,烧杯②看盛有碳酸钠
粉末。为了验证使石蕊变色的物质是碳酸而不是二氧
化碳,应采取的实验操作是
。
⑶ 若先将甲中的液体挤出,观察出气球明显鼓起,一段时间后恢复原状;再将乙中的液体挤出,气球又明显鼓起。请将下表中的试剂补充完整。
| 滴管甲 | 烧杯① | 滴管乙 | 烧杯② | |
| 试剂 | H2O | Mg |
气球鼓起是因为装置内气压增大,两次气压增大的原因依次是
。

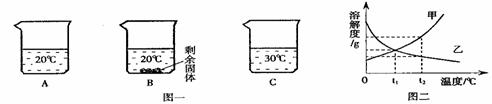 向装有等量水的A、B、C烧杯中分别加入10g、25g、25gNaNO3固体,充分溶解后,现象如图一所示。
向装有等量水的A、B、C烧杯中分别加入10g、25g、25gNaNO3固体,充分溶解后,现象如图一所示。