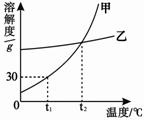
过氧化钠是化学中常见的一种药品,它是浅黄色颗粒。易溶于水,能与水发生反应,生成氢氧化钠和过氧化氢,化学方程式:Na2O2+2H2O=2NaOH+H2O2,过氧化氢又能 分解放出氧气。
(1)区分水和过氧化氢的实验方法是: ,发生的反应方程式是:_______ ____。
(2)某同学为了证明过氧化钠加入水中生成了氢氧化钠,在生成的溶液中滴加了几滴无色酚酞试液,观察到的现象是溶液先变红后褪为无色,请你对此现象进行探究。
【提出问题】:什么原因导致溶液变红后再褪色的呢?
【猜想与假设】:
猜想1:甲同学“可能是无色酚酞溶液变质导致溶液褪色”;
猜想2:乙同学“可能是生成的过氧化氢使溶液褪色”。
【实验与结论】:
a:甲同学提出的猜想,立即遭到其他同学的反对,因为 ;
b:为了验证自己的猜想,乙同学设计了以下方案并实验验证:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量稀氢氧化钠溶液于试管中,滴加1—2滴酚酞试液,变红后 观察现象 | 溶液依然 为红色 |
|
【讨论交流】:你还能提出不同的猜想吗?如果还能提出新的合理的假设和方案你将获得奖励分4分。(化学试卷总分不超过60分)
猜想3: 。
方案3:
| 实验步骤 | 实验现象 | 实验结论 |
 D.空气
D.空气
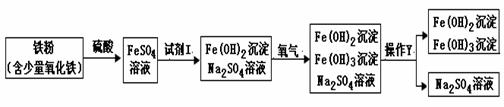 下图是氧化沉淀法生产复印用高档Fe3O4粉的部分工艺流程简图。
下图是氧化沉淀法生产复印用高档Fe3O4粉的部分工艺流程简图。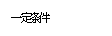 ⑶钛是一种密度小、熔点高、耐腐蚀的优良金属,有“未来金属”的美誉,工业上冶炼钛的
⑶钛是一种密度小、熔点高、耐腐蚀的优良金属,有“未来金属”的美誉,工业上冶炼钛的