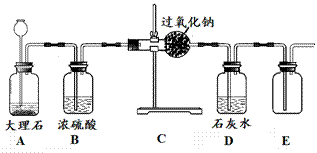
(9分)已知某金属粉末中可能含有铁、铝、铜三种金属中的两种或三种,化学小组的同学对该粉末进行探究。
【提出猜想】
猜想一:该粉末由铜、铝组成; 猜想二:该粉末由铁、铝组成;
猜想三:该粉末由铁、铝、铜组成; 猜想四:该粉末由 ▲ 组成。
【查阅资料】铝与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气,反应的化学方程式为2Al + 2H2O + 2NaOH =" 2NaAlO2" + 3H2↑,铁和铜与氢氧化钠溶液均不发生反应。
【供选药品】稀盐酸、稀硫酸、氢氧化钠溶液、硫酸铜溶液、澄清石灰水、蒸馏水。
【进行实验】
【反思与评价】若将原粉末中的铜全部回收,请写出实验过程 ▲ 。
【提出猜想】
猜想一:该粉末由铜、铝组成; 猜想二:该粉末由铁、铝组成;
猜想三:该粉末由铁、铝、铜组成; 猜想四:该粉末由 ▲ 组成。
【查阅资料】铝与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气,反应的化学方程式为2Al + 2H2O + 2NaOH =" 2NaAlO2" + 3H2↑,铁和铜与氢氧化钠溶液均不发生反应。
【供选药品】稀盐酸、稀硫酸、氢氧化钠溶液、硫酸铜溶液、澄清石灰水、蒸馏水。
【进行实验】
| 实验目的 | 实验操作 | 实验现象 | 实验结论 |
| 证明粉末中是否含有 ▲ | 取一个小烧杯,加入适量的粉末,再向其中加入足量的 ▲ | ▲ | 猜想四成立; 实验中发生反应 的化学方程式为 ▲ |
| 证明粉末中是否含有 ▲ | 过滤,将得到的固体洗涤后放入小烧杯,再向其中加入足量的稀盐酸 | ▲ |
(3分)为测定某碳酸钠样品(其中杂质不溶于水)纯度,进行了以下实验:取48 g样品加入水使碳酸钠完全溶解后除去杂质,将得到的液体平均分为四份,每份中分别加入一定质量的氯化钙溶液,反应的化学方程式为CaCl2 + Na2CO3 =" CaCO3↓+" 2NaCl,实验数据见下表。
请计算:
⑴每份液体完全反应时,生成沉淀的质量为 ▲ g。
⑵样品中碳酸钠的纯度。
| | 第一份 | 第二份 | 第三份 | 第四份 |
| 加入CaCl2溶液的质量/g | 10 | 20 | 30 | 40 |
| 生成沉淀的质量/g | 4 | 8 | 10 | 10 |
⑴每份液体完全反应时,生成沉淀的质量为 ▲ g。
⑵样品中碳酸钠的纯度。
下列变化中,属于化学变化的是
| A.西瓜榨成西瓜汁 | B.水加热成为水蒸气 |
| C.铝块压制成铝箔 | D.玉米发酵制成酒精 |
“A D钙奶”中,“钙”指的是
| A.单质 | B.元素 | C.原子 | D.分子 |
下列物质中,不会造成空气污染的是
| A.可吸入颗粒物 | B.氧气 | C.二氧化硫 | D.二氧化氮 |
下列做法不正确的是
0 53071 53079 53085 53089 53095 53097 53101 53107 53109 53115 53121 53125 53127 53131 53137 53139 53145 53149 53151 53155 53157 53161 53163 53165 53166 53167 53169 53170 53171 53173 53175 53179 53181 53185 53187 53191 53197 53199 53205 53209 53211 53215 53221 53227 53229 53235 53239 53241 53247 53251 53257 53265 211419
| A.电器起火时,用水扑灭 | B.乘坐公交车时,不携带鞭炮 |
| C.油锅起火时,盖上锅盖 | D.厨房燃气灶漏气时,应关闭阀门,打开窗户 |