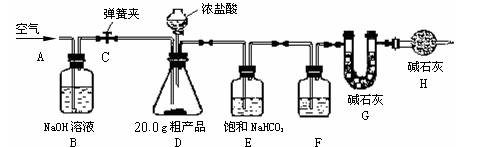
下列物质的变化属于物理变化的是
( )
( )
| A.火烧赤壁 | B.干冰升华 | C.淀粉水解 | D.铁钉生锈 |
合理施肥是农业生产和城市绿化建设的重要措施。下列化肥属于钾肥的是 ( )
| A.CO(NH2)2 | B.NH4HCO3 | C.K2SO4 | D.NH4H2PO4 |
2009年中央电视台春节联欢晚会中,台湾魔术师刘谦以其匪夷所思的表演震撼了国人,他表演过程使用的道具中,由金属材料制成的是 ( )
| A.玻璃杯 | B.金戒指 | C.扑克牌 | D.橡皮筋 |
市政府有关部门提醒大家,冬季用燃气热水器洗澡要特别注意室内通风,以免造成人员中毒。这里的有毒气体主要是指 ( )
| A.CO2 | B.N2 | C.O2 | D.CO |
下列实验现象的描述不正确的是 ( )
| A.NaOH溶液加入CuSO4溶液生成蓝色沉淀 | B.打开浓盐酸的瓶盖,有白烟冒出 |
| C.硫在氧气中燃烧,产生蓝紫色火焰 | D.镁条在空气中燃烧,发出耀眼的白光 |
小伟同学探究金属单质的活泼性时发现:X、Y都能与稀硫酸反应放出氢气而Z不能;Y能在X的盐溶液中置换出X。则它们的金属活动顺序为 ( )
| A.X>Y>(H)>Z | B.Y>X>(H)>Z | C.X>Z>(H)>Y | D.Y>(H)>X> Z |
自来水厂净水流程为:天然水 沉降
沉降 过滤
过滤 吸附
吸附 自来水,沉降过程中常用作絮凝剂的物质是 ( )
自来水,沉降过程中常用作絮凝剂的物质是 ( )
 沉降
沉降 过滤
过滤 吸附
吸附 自来水,沉降过程中常用作絮凝剂的物质是 ( )
自来水,沉降过程中常用作絮凝剂的物质是 ( )| A.明矾 | B.活性炭 | C.氯气 | D.漂白粉 |
某化学兴趣小组以“太湖水污染情况调查”为课题进行研究性学习,为了较准地测定湖水样品的酸碱度,可以使用 ( )
0 52738 52746 52752 52756 52762 52764 52768 52774 52776 52782 52788 52792 52794 52798 52804 52806 52812 52816 52818 52822 52824 52828 52830 52832 52833 52834 52836 52837 52838 52840 52842 52846 52848 52852 52854 52858 52864 52866 52872 52876 52878 52882 52888 52894 52896 52902 52906 52908 52914 52918 52924 52932 211419
| A.石蕊试液 | B.酚酞试液 | C.pH试纸 | D.铁粉 |