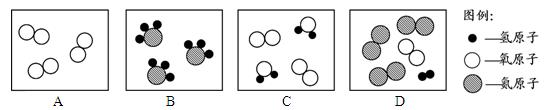
下列字母表示的各种物质是初中化学常见的不同物质。其中A、B、C、D存在如图所示的转化关系(其中“→”表示可以进行转化),四种物质中均含有两种相同的元素。

(1)B是纯碱,其化学式为 。
(2)X是由三种元素组成的酸,请写出X与B反应生成D、Y和Z的化学方程式 。
(3)A在受热时可以分解生成B、Y和Z,那么A的化学式为 。
(4)向A的溶液中加入C的溶液,可以生成B和Z,请写出该化学方程式 。
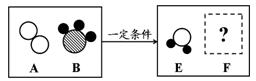
(5)从上述物质中选2种为一组,按下图所示装置进行实验。将胶头滴管中的液体滴入瓶中,看到烧杯中的澄清石灰水变浑浊。写出符合要求的两组物质。

(6)请根据以上七种物质分析,下列说法正确的是 。
a.X与A、B、C反应均有气泡冒出 b.七种物质中A、B、D属于盐类
c.Y与C反应可以生成B和Z d.X、Y、Z的相对分子质量依次减小

(1)B是纯碱,其化学式为 。
(2)X是由三种元素组成的酸,请写出X与B反应生成D、Y和Z的化学方程式 。
(3)A在受热时可以分解生成B、Y和Z,那么A的化学式为 。
(4)向A的溶液中加入C的溶液,可以生成B和Z,请写出该化学方程式 。
(5)从上述物质中选2种为一组,按下图所示装置进行实验。将胶头滴管中的液体滴入瓶中,看到烧杯中的澄清石灰水变浑浊。写出符合要求的两组物质。
| 物质 序号 | 液体 | 固体 |
| ① | | |
| ② | | |

(6)请根据以上七种物质分析,下列说法正确的是 。
a.X与A、B、C反应均有气泡冒出 b.七种物质中A、B、D属于盐类
c.Y与C反应可以生成B和Z d.X、Y、Z的相对分子质量依次减小
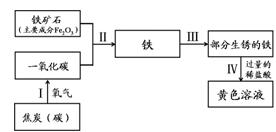
某化学兴趣小组对水蒸气通过灼热的焦炭后,得到的混合气体主要成分产生了兴趣。同学们决定通过实验进行探究。
【提出猜想】该混合气体主要成分为一氧化碳、二氧化碳、氢气和水蒸气。
【查阅资料】a.无水硫酸铜遇水由白色变为蓝色。
b.碱石灰是固体氢氧化钠和氧化钙的混合物。
c.氢气、一氧化碳均能在加热的条件下与氧化铜反应。
【实验过程】同学们在老师的指导下设计了如下图所示装置,并进行了实验(部分夹持仪器已略去)。
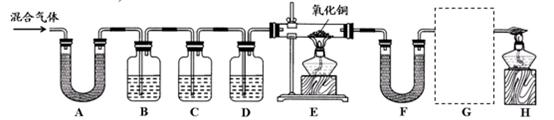
(1)装置A中无水硫酸铜变蓝,装置B中澄清石灰水变浑浊。由此得出的结论为 。写出装置B中反应的化学方程式 。
(2)装置C和D中的药品分别为 。
(3)同学们通过观察装置E、F中的现象后,证明了混合气中含有氢气。为了证明第四种气体的存在,装置G中的药品、现象和结论是 。
【实验结论】猜想正确。
【实验反思】
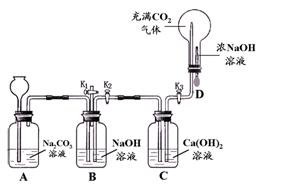
经过讨论,同学们将上图中装置C~H进行了简化,改进后的装置如下图所示。
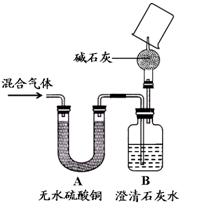
(3)干燥管中碱石灰的作用为 。
(4)同学们为了验证通过干燥管后气体的成分,继续进行的实验为:
【提出猜想】该混合气体主要成分为一氧化碳、二氧化碳、氢气和水蒸气。
【查阅资料】a.无水硫酸铜遇水由白色变为蓝色。
b.碱石灰是固体氢氧化钠和氧化钙的混合物。
c.氢气、一氧化碳均能在加热的条件下与氧化铜反应。
【实验过程】同学们在老师的指导下设计了如下图所示装置,并进行了实验(部分夹持仪器已略去)。

(1)装置A中无水硫酸铜变蓝,装置B中澄清石灰水变浑浊。由此得出的结论为 。写出装置B中反应的化学方程式 。
(2)装置C和D中的药品分别为 。
(3)同学们通过观察装置E、F中的现象后,证明了混合气中含有氢气。为了证明第四种气体的存在,装置G中的药品、现象和结论是 。
【实验结论】猜想正确。
【实验反思】
经过讨论,同学们将上图中装置C~H进行了简化,改进后的装置如下图所示。

(3)干燥管中碱石灰的作用为 。
| | 实验操作 | 实验现象 | 实验结论 |
| ① | 在尖嘴处点燃气体, 。 | 。 | 。 |
| ② | 。 | 。 | 。 |
日常生活中发生的下列变化,属于化学变化的是
0 52679 52687 52693 52697 52703 52705 52709 52715 52717 52723 52729 52733 52735 52739 52745 52747 52753 52757 52759 52763 52765 52769 52771 52773 52774 52775 52777 52778 52779 52781 52783 52787 52789 52793 52795 52799 52805 52807 52813 52817 52819 52823 52829 52835 52837 52843 52847 52849 52855 52859 52865 52873 211419
| A.蜡烛燃烧 | B.纸张粉碎 | C.冰雪融化 | D.酒精挥发 |