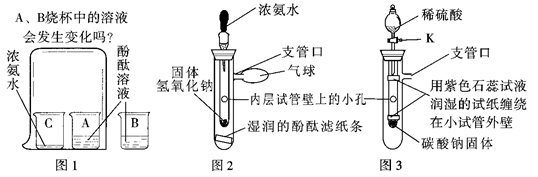
(10贵港21)某化学小组发现一袋包装破损的漂白粉,同学们对其漂白作用是否失效产生了疑问。
【查阅资料】漂白粉的主要成分是Ca(ClO)2、CaCl2和Ca(OH)2,其有效成分是Ca(ClO)2。Ca(ClO)2可溶于水,漂白原理是:它在空气中发生反应Ca(ClO)2+H2O+CO2=CaCO3+2HClO,HClO能使有色物质如品红溶液褪色。HClO不稳定,易分解生成HCl和O2。
【实验探究】
【继续探究】同学们对失效后的漂白粉的成分很感兴趣,并作进一步探究。在老师的帮助下,同学们对失效后的漂白粉成分进行猜想,猜想一:CaCl2和CaCO3;猜想二:CaCl2和Ca(OH)2;猜想三:CaCl2和CaCO3和Ca(OH)2。
【查阅资料】漂白粉的主要成分是Ca(ClO)2、CaCl2和Ca(OH)2,其有效成分是Ca(ClO)2。Ca(ClO)2可溶于水,漂白原理是:它在空气中发生反应Ca(ClO)2+H2O+CO2=CaCO3+2HClO,HClO能使有色物质如品红溶液褪色。HClO不稳定,易分解生成HCl和O2。
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| 把少量漂白粉样品加入水中,通入足量的CO2气体,___________________。 | ______________________。 | 漂白粉的漂白作用已失效。 |
【继续探究】同学们对失效后的漂白粉的成分很感兴趣,并作进一步探究。在老师的帮助下,同学们对失效后的漂白粉成分进行猜想,猜想一:CaCl2和CaCO3;猜想二:CaCl2和Ca(OH)2;猜想三:CaCl2和CaCO3和Ca(OH)2。
| 实验操作 | 实验现象 | 实验结论 |
| 步骤一:把样品加入水中,充分溶解后过滤, ________________________________。 | 有气泡产生。 | 猜想一成立。 |
| 步骤二:________________________________。 | ______________________。 |
(10成都18)木炭作为还原剂用于金属冶炼已有几千年历史。教材用如图I实验介绍这一知识。
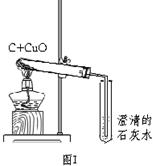
(1)木炭与氧化铜反应的化学方程式是______________________________;
(2)木炭呈块状,实验时要先将木炭研细,再与CuO粉末混合均匀后使用。这样处理的目的是______________________________________
(3)酒精灯火焰处加有铁丝网罩,其作用时_______________________
(4)为了提高成功率,某研究小组设计如图Ⅱ方案进行实验。
【装置改进】
稳定的高温时本实验成果的关键因素之一,实验装置也会影响加热的效率。图Ⅱ装置将卧式装置改为直立式装置。实验时,将反应混合物夯实于试管底部,调节酒精灯是外焰完全包围试管的下部。你认为该设计是否更好?____________(填“是”或“否”);理由是________________________________________________;
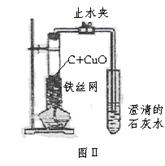
【实验研究】
分别称取2g木炭与CuO的混合物,按每种比例重复实验3次。实验记录如下表:
总质量相同(2g)但木炭与CuO比例不同的实验对比表
由实验数据分析,影响实验的另一因素是______________________________;从产物分析,该反应混合物的最佳比例范围是_____________________;
【讨论交流】
由于试管中有空气,实验时应注意:
① 混合物需进行预热,除了使试管受热均匀外,目的是_______________________________;
② 不能把石灰水浑浊作为木炭跟CuO反应的充分证据。因为试管中还可能发生反应:
___________________________________(写化学方程式)
【提出问题】关于影响该实验的因素,你认为还可进一步探究的问题

(1)木炭与氧化铜反应的化学方程式是______________________________;
(2)木炭呈块状,实验时要先将木炭研细,再与CuO粉末混合均匀后使用。这样处理的目的是______________________________________
(3)酒精灯火焰处加有铁丝网罩,其作用时_______________________
(4)为了提高成功率,某研究小组设计如图Ⅱ方案进行实验。
【装置改进】
稳定的高温时本实验成果的关键因素之一,实验装置也会影响加热的效率。图Ⅱ装置将卧式装置改为直立式装置。实验时,将反应混合物夯实于试管底部,调节酒精灯是外焰完全包围试管的下部。你认为该设计是否更好?____________(填“是”或“否”);理由是________________________________________________;

【实验研究】
分别称取2g木炭与CuO的混合物,按每种比例重复实验3次。实验记录如下表:
总质量相同(2g)但木炭与CuO比例不同的实验对比表
| 比例 | 1:6 | 1:7 | 1:8 | 1:9 | 1:10~1:11 | 1:12 | 1:13 |
| 加热时间 | 1′51″ | 1′43″ | 1′57″ | 1′51″ | 1′51″ | 1′53″ | 4′ |
| 实验现象 | 红热,产生大量气泡,石灰水变浑浊 | 偶尔红热,气泡较少 | |||||
| 实验结果 | 表层铜珠较大,出现未完全反应的黑色木炭粉末,且木炭含量越高黑色粉末越多 | 反应较完全,生成亮红色网状铜块 | 部分生成Cu2O | 主要产物是Cu2O |
由实验数据分析,影响实验的另一因素是______________________________;从产物分析,该反应混合物的最佳比例范围是_____________________;
【讨论交流】
由于试管中有空气,实验时应注意:
① 混合物需进行预热,除了使试管受热均匀外,目的是_______________________________;
② 不能把石灰水浑浊作为木炭跟CuO反应的充分证据。因为试管中还可能发生反应:
___________________________________(写化学方程式)
【提出问题】关于影响该实验的因素,你认为还可进一步探究的问题
.(10连云港27)某研究性学习兴趣小组同学在学习了酸、碱、盐的知识后,走进化学实验室。邀请你参与以下活动。(已知①2Na2CO3+ H2SO4==NaHCO3+Na2SO4 NaHCO3 溶液呈碱性②CaSO4微溶,但在稀溶液中看作可溶,其水溶液呈中性)
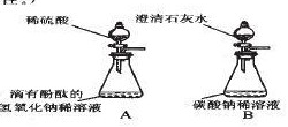
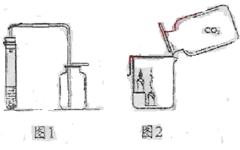
(1)甲、乙两同学想用实验证明稀硫酸和NaOH稀溶液确实能发生反应,设计了如图A所示的实验。丙、丁两同学想再现课本上将“澄清的石灰水滴入Na2CO3溶液”的现象,设计了如图B所示的实验,并各自进行操作。
【问题讨论】教师首先肯定了这四位同学的实验设计和操作,请你填空:
甲、乙同学将较多量的稀硫酸加入锥形瓶后,他们是依据溶液的颜色由 色变为 色的现象来判断两者确实发生反应的。丙、丁同学的实验中发生的复分解反应可用化学方程式表示
为
【意外发现】甲同学和丙同学在洗刷仪器前,将A、B装置锥形瓶中的残留物倒入同一个洁净的废液缸,发现白色沉淀溶解,有气泡产生,废液缸中形成无色溶液,这一现象立刻引起了同学们的好奇。于是,他们又以“无色溶液中含有那些溶质”为课题进行研究。
【提出猜想】经讨论呈现出如下猜想:
①溶质为:Na2SO4 CaSO4
②溶质为:Na2SO4 CaSO4 H2SO4
③溶质为:Na2SO4 CaSO4 NaOH
请你判断:上述猜想中不合理的是 (填数字代号)
【实验探究】小组同学针对认为合理的猜想,设计实验进行探究,请你将下表补充完整。
【意外发现2】乙同学和丁同学在洗刷仪器前,将A、B装置锥形瓶中的残留物倒入另一个洁净的废液缸,发现沉淀不溶,没有气泡,上层清液呈红色。此时,上层清液中溶质的组成情况可能有许多组。如①Na2SO4 NaOH ②Na2SO4 Ca(OH)2③Na2SO4 NaOH Na2CO3
④Na2SO4 ⑤Na2SO4 Na2CO3 (未列全。请用化学式将④⑤补充完整)
(2)教师点拨:证明稀硫酸和NaOH稀溶液确实能发生反应的方法还有多种。
【拓展探究】小组同学用其他装置继续进行实验。请你回答下列问题
①若不加酚酞试液,将稀硫酸(适量)与NaOH稀溶液混合后,再向其中加入CuSO4溶液至蓝色 沉淀生成,则(填“能”或“不能”)证明两者确实发生了反应。
②若不加酚酞试液,将稀硫酸(少量)与V1mLNaOH稀溶液混合后,再向其中CuSO4溶液至蓝色沉淀不再产生时,消耗了V2mLCuSO4溶液,此时还必须做一个对比实验才能证明两者确实发生了反应,这个对比实验是(简述操作方法及结论)证明稀硫酸和NaOH稀溶液确实发生了反应。

(1)甲、乙两同学想用实验证明稀硫酸和NaOH稀溶液确实能发生反应,设计了如图A所示的实验。丙、丁两同学想再现课本上将“澄清的石灰水滴入Na2CO3溶液”的现象,设计了如图B所示的实验,并各自进行操作。
【问题讨论】教师首先肯定了这四位同学的实验设计和操作,请你填空:
甲、乙同学将较多量的稀硫酸加入锥形瓶后,他们是依据溶液的颜色由 色变为 色的现象来判断两者确实发生反应的。丙、丁同学的实验中发生的复分解反应可用化学方程式表示
为
【意外发现】甲同学和丙同学在洗刷仪器前,将A、B装置锥形瓶中的残留物倒入同一个洁净的废液缸,发现白色沉淀溶解,有气泡产生,废液缸中形成无色溶液,这一现象立刻引起了同学们的好奇。于是,他们又以“无色溶液中含有那些溶质”为课题进行研究。
【提出猜想】经讨论呈现出如下猜想:
①溶质为:Na2SO4 CaSO4
②溶质为:Na2SO4 CaSO4 H2SO4
③溶质为:Na2SO4 CaSO4 NaOH
请你判断:上述猜想中不合理的是 (填数字代号)
【实验探究】小组同学针对认为合理的猜想,设计实验进行探究,请你将下表补充完整。
| 实验内容 | 实验现象和结论 |
| 取废液缸中少量溶液于试管中,滴入 少量 溶液,观察 | a.若有气泡产生,则猜想 成立 |
| b.若无气泡产生,则猜想 成立 |
【意外发现2】乙同学和丁同学在洗刷仪器前,将A、B装置锥形瓶中的残留物倒入另一个洁净的废液缸,发现沉淀不溶,没有气泡,上层清液呈红色。此时,上层清液中溶质的组成情况可能有许多组。如①Na2SO4 NaOH ②Na2SO4 Ca(OH)2③Na2SO4 NaOH Na2CO3
④Na2SO4 ⑤Na2SO4 Na2CO3 (未列全。请用化学式将④⑤补充完整)
(2)教师点拨:证明稀硫酸和NaOH稀溶液确实能发生反应的方法还有多种。
【拓展探究】小组同学用其他装置继续进行实验。请你回答下列问题
①若不加酚酞试液,将稀硫酸(适量)与NaOH稀溶液混合后,再向其中加入CuSO4溶液至蓝色 沉淀生成,则(填“能”或“不能”)证明两者确实发生了反应。
②若不加酚酞试液,将稀硫酸(少量)与V1mLNaOH稀溶液混合后,再向其中CuSO4溶液至蓝色沉淀不再产生时,消耗了V2mLCuSO4溶液,此时还必须做一个对比实验才能证明两者确实发生了反应,这个对比实验是(简述操作方法及结论)证明稀硫酸和NaOH稀溶液确实发生了反应。
(10天津市26).今春我国西南大部分地区发生严重的旱灾,我们在抗旱救灾的同时,更应倡导保护水环境、珍惜水资源。请回答下列问题:
(1)不论是自来水还是纯净水,你认为保持水化学性质的最小粒子是______。下列选项中能确认水是由氢元素和氧元素组成的实验是__________(填序号,下同)。
A.水的蒸馏 B.水的蒸发 C.水的电解 D.水的净化
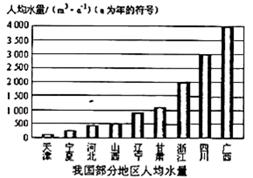
(2)右图是我国部分地区人均水量图,从中可以看出我市是极度缺水的城市。下列做法符合节约用水的是_____。
A.使用节水龙头
B.用淘米水洗碗
C.用喷灌、滴灌方法给农作物浇水
D.使用不间断地边注水边冲淋、排水的用水量为165L/次的家用洗衣机
(3)实验室中有一杯含有MgCl2和CaCl2的硬水,下表是某兴趣小组设计软化硬水的实验方案,请你一起来完成下表。
可供选用的药品有:Ca(OH)2溶液、NaOH溶液、Na2CO3溶液、肥皂水
(1)不论是自来水还是纯净水,你认为保持水化学性质的最小粒子是______。下列选项中能确认水是由氢元素和氧元素组成的实验是__________(填序号,下同)。
A.水的蒸馏 B.水的蒸发 C.水的电解 D.水的净化
(2)右图是我国部分地区人均水量图,从中可以看出我市是极度缺水的城市。下列做法符合节约用水的是_____。

A.使用节水龙头
B.用淘米水洗碗
C.用喷灌、滴灌方法给农作物浇水
D.使用不间断地边注水边冲淋、排水的用水量为165L/次的家用洗衣机
(3)实验室中有一杯含有MgCl2和CaCl2的硬水,下表是某兴趣小组设计软化硬水的实验方案,请你一起来完成下表。
可供选用的药品有:Ca(OH)2溶液、NaOH溶液、Na2CO3溶液、肥皂水
| 实验操作 | 现象 | 结论或化学方程式 |
| ①取少量硬水样品于试管中,向其中滴加:Ca(OH)2溶液,直到不再产生沉淀 | 有白色沉淀产生 |  MgCl2+ Ca(OH)2== Mg(OH)2 +CaCl2 MgCl2+ Ca(OH)2== Mg(OH)2 +CaCl2 |
| ②再向上述试管中滴加______,直到不再产生沉淀 | 有白色沉淀产生 | 化学方程式:____________ |
| ③过滤 | 滤出沉淀 | 得到澄清滤液 |
| ④用两试管分别取等量的上述滤液和原硬水样品,分别滴加____,振荡 | 盛有滤液的试管中________ | 证明硬水已软化 |
【10福建宁德17】.(11分)一包黑色粉末可能由氧化铜和炭粉中的一种或两种物质组成,某学校科学小组为确定其成分,进行了以下探究活动:
【查阅资料】硫酸铜溶液呈蓝色
【设计方案】(1)取少量黑色粉末于试管中 观察现象
观察现象
实验中可能出现的现象与对应结论如下表,请你完成下表中①②相关内容:
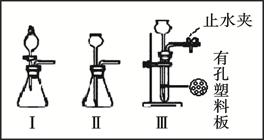
(2)通过实验及分析,确定该粉末为氧化铜和炭粉的混合物,为了进一步探究它们的性质,探究小组又利用这种混合物补充做了如下图所示实验:

①能证明CuO与C已发生化学反应的实验现象是 。(答一点即可)试管b中反应的化学方程式为 。
②最能说明试管中物质已完全反应的实验现象是
【查阅资料】硫酸铜溶液呈蓝色
【设计方案】(1)取少量黑色粉末于试管中
 观察现象
观察现象实验中可能出现的现象与对应结论如下表,请你完成下表中①②相关内容:
| 现象 | 结论 |
| 溶液呈蓝色,有黑色不溶物 | 含CuO、C |
| 溶液颜色无明显变化,有黑色不溶物 | 只含① |
| 溶液呈蓝色,② 。 | 只含CuO |
(2)通过实验及分析,确定该粉末为氧化铜和炭粉的混合物,为了进一步探究它们的性质,探究小组又利用这种混合物补充做了如下图所示实验:

①能证明CuO与C已发生化学反应的实验现象是 。(答一点即可)试管b中反应的化学方程式为 。
②最能说明试管中物质已完全反应的实验现象是
【10湖北十堰21】.小丹同学在学习酸的性质时,从同一卷镁带中剪取长度相等的两根镁带,分别与室温下H浓度相同的稀盐酸、稀硫酸反应。观察发现:镁带在稀盐中放出气泡的速率明显快鱼在稀硫酸中防除气泡的速率。
[查阅资料]
1.金属与酸发生置换反映,基本质是金属单质与H反映。
2.生成H2速率主要取决与:①金属表面积 ②溶液中H浓度 ③温度等条件
3.H的浓度与1L溶液中H的数目成正比。
4.溶液中除H外的其它离子可能会影响反映速率。
[提出问题]
①小丹同学在进行上述实验时,控制了镁带与酸反映的哪几个条件?(答出两条)
②上述反映中C1-、SO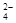 如果反映速度?
如果反映速度?
[猜想假设]
I.Cl-促进了镁与酸的反映,SO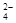 对反映无影响。
对反映无影响。
II.SO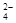 抑制了镁与酸的反映,C1-对反映无影响。
抑制了镁与酸的反映,C1-对反映无影响。
III. 。
请回答问题①,完成猜想3
[实验探究]为了验证猜想,小丹设计了如下实验:
试剂B是 (化学式)固体。
[结论]结论A为 。
[反思]将试剂B改用HC1气体,不能达到探究目的,其原因是 。
0 51908 51916 51922 51926 51932 51934 51938 51944 51946 51952 51958 51962 51964 51968 51974 51976 51982 51986 51988 51992 51994 51998 52000 52002 52003 52004 52006 52007 52008 52010 52012 52016 52018 52022 52024 52028 52034 52036 52042 52046 52048 52052 52058 52064 52066 52072 52076 52078 52084 52088 52094 52102 211419
[查阅资料]
1.金属与酸发生置换反映,基本质是金属单质与H反映。
2.生成H2速率主要取决与:①金属表面积 ②溶液中H浓度 ③温度等条件
3.H的浓度与1L溶液中H的数目成正比。
4.溶液中除H外的其它离子可能会影响反映速率。
[提出问题]
①小丹同学在进行上述实验时,控制了镁带与酸反映的哪几个条件?(答出两条)
②上述反映中C1-、SO
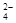 如果反映速度?
如果反映速度?[猜想假设]
I.Cl-促进了镁与酸的反映,SO
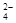 对反映无影响。
对反映无影响。II.SO
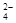 抑制了镁与酸的反映,C1-对反映无影响。
抑制了镁与酸的反映,C1-对反映无影响。III. 。
请回答问题①,完成猜想3
[实验探究]为了验证猜想,小丹设计了如下实验:
| 实验 编号 | 铝片 长度 | H+浓度 相同的酸 | 反应片刻后 添加少量试剂 | 产生气泡 的速率 | 结论 |
| A | 2cm | 5mL盐酸 | Na2SO4固体 | 无明显变化 | (结论A) |
| B | 2cm | 5mL硫酸 | (试剂B) | 明显加快 | Cl-对反应有促进作用 |
试剂B是 (化学式)固体。
[结论]结论A为 。
[反思]将试剂B改用HC1气体,不能达到探究目的,其原因是 。
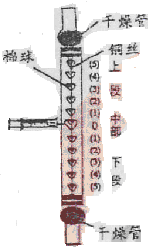
 认为是CO,丙认为是Na2CO3,丁认为是CO和Na2CO3,戊认为是NaHCO
认为是CO,丙认为是Na2CO3,丁认为是CO和Na2CO3,戊认为是NaHCO 3。为确定该反应的含碳产物,五位同学用右图装置进行实验探究。
3。为确定该反应的含碳产物,五位同学用右图装置进行实验探究。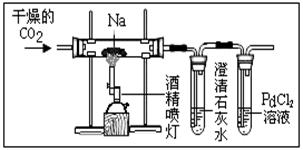
 ________。
________。