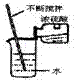现有银、铜、铁三种金属,某研究小组的同学为探究银、铜、铁的金属活动性顺序,设计了三个实验:I.将铁片浸入稀硫酸中;II.将银片浸入稀硫酸中;III.将铁片浸入硫酸铜溶液中。
(1)实验I的现象是:有气泡产生,溶液由无色逐渐变为浅绿色。反应的化学方程式为 ;反应产生的气体可用 的方法检验。
(2)上述三个实验还不能完全证明三种金属的活动性顺序,请你补充一个实验来达到实验目的(写出实验操作和现象) 。根据以上探究,三种金属的活动性由强到弱的顺序是 。
(3)将银、铜、铁中的两种金属分别放入 溶液中,即可验证这三种金属的活动性强弱。
(4)将铜片加热,铜片表面变黑。同学们设计如下实验证明此黑色物质是氧化铜。
| ①实验操作 | ②实验现象 |
| 剪下一片变黑的铜片,放入试管中,加入足量的 溶液。 | 铜片表面的黑色物质全部消失,露出红色的铜,溶液变为 色。 |
请根据下图所示实验装置回答问题:
 |
(1)写出图中标号仪器的名称:a ,b 。
(2)实验室若用装置A制取氧气,则发生反应的化学方程式为 。若用装置B制取氧气,药品选用高锰酸钾,则发生反应的化学方程式为 ,在试管口放一团棉花的作用是 。
(3)实验室收集二氧化碳选用装置 (填序号)。若收集某气体只能采用装置E,由此推测该气体具有的性质是 。
粗盐中含有MgCl2、CaCl2等杂质,工业提纯粗盐的工艺流程如下图所示:
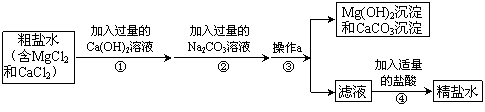 |
(1)Ca(OH)2溶液的pH (填“>”、“=”或“<”)7。步骤①反应的化学方程式为 。
(2)步骤③操作a的名称是 。步骤④加入适量盐酸的目的是除去滤液中的Na2CO3和 。
(3)若步骤①和步骤②的顺序颠倒,则最后所得的精盐水中还含有 。
下表是NaCl、NH4Cl在不同温度时的溶解度。
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | |
| 溶解度/ g | NaCl | 35.7 | 36.0学科王 | 36.6学科王 | 37.3学科王 | 38.4 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | |
(1)以上两种物质溶解度的变化受温度影响较小的是 。
(2)20℃时,将40gNaCl加入到100g水中充分搅拌后,所得溶液的质量为 g。
(3)40℃时,要使接近饱和的NH4Cl溶液变为饱和溶液,下列方法中一定能达到目的的是 (填序号)。
① 升高温度 ②加溶质NH4Cl ③加水 ④恒温蒸发水
 B.
B. C.
C. D.
D.