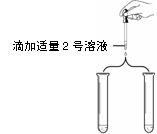
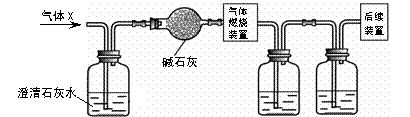
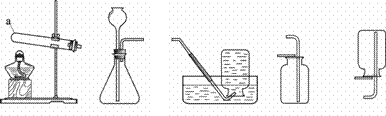
化学兴趣小组同学发现实验台上按如下顺序摆放着7瓶不同的无色溶液(如图所示),其中4、5号试剂瓶标签破损。
 |
1 2 3 4 5 6 7
【提出问题】这两瓶试剂的成分分别是什么?
【查阅资料】①碱性的亚硫酸钠(Na2SO3)溶液、Na2CO3溶液与中性的CaCl2溶液均可发生复分解反应,产生白色沉淀。
②Na2SO3 + 2HCl=2NaCl + SO2↑ + H2O。
③CO2与SO2均可以使澄清石灰水变浑浊。
【作出猜想】根据受损标签的信息,推测4、5号溶液可能分别是NaOH溶液、Na2CO3溶液、Na2SO3溶液或NaCl溶液中的一种。
【实施方案】各取少量4、5号溶液于试管中,分别进行下列两组实验。
| 实验操作 | 实验现象 | 实验结论 |
|
| 溶液均由无色变成红色 | 4、5号溶液均不可能是上述猜想中的 溶液。 |
|
| 均产生白色沉淀 | 4、5号溶液可能分别是Na2SO3溶液和Na2CO3溶液中的一种。写出其中一个反应的化学方程式 |
【继续实验】为了进一步确定4、5号溶液的成分,同学们分别取少量4、5号![]() 溶液于试管中继续实验。
溶液于试管中继续实验。
| 实验操作 | 实验现象 | 实验结论 |
|
| _____ | 4号溶液是Na2CO3溶液 5号溶液是Na2SO3溶液。 |
【实验反思】同学们经过分析认为4号溶液还可能是变质的NaOH溶液。于是设计了以下实验方案进行验证。请完成下列实验报告。
| 实验操作 | 实验现象 | 实验结论 |
| 4号溶液是部分变质的NaOH溶液。 |
溶液的应用非常广泛。
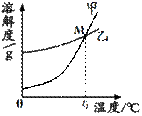 (1)K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如下。
(1)K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如下。
| 温度/℃ | 20 | 30 | 50 | 60 | 80 | |
| 溶解度/g | K2CO3 | 110 | 114 | 121 | 126 | 139 |
| KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 | |
①图中能表示KNO3溶解度曲线的是 (填“甲”或“乙”)。
②曲线上M点的含义是 。
③20℃时,K2CO3饱和溶液中溶质与溶剂的质量比为 (结果用最简整数比表示)。
④30![]() ℃时,向114 g K2CO3固体中加入100 g水,充分溶解后升温至40℃,该溶液中溶质的质量分数 (填“变大”、“变小”或“不变”)。
℃时,向114 g K2CO3固体中加入100 g水,充分溶解后升温至40℃,该溶液中溶质的质量分数 (填“变大”、“变小”或“不变”)。
(2)某KNO3样品中含有少量K2CO3,其提纯过程如下:
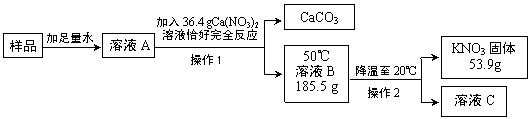 |
小资料:K2CO3 + Ca(NO3)2 = CaCO3↓+ 2KNO3
①操作2的名称是 。
②溶液B和溶液C中属于饱和溶液的是 (填序号)。
③样品中钾元素的质量为 g(结果保留整数)。
 实验1
实验1 实验2
实验2