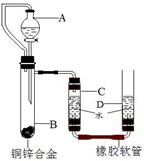
有一均匀的颗粒状的铜锌合金Wg,小明用下图装置,通过测定合金与酸反应产生氢气的体积来测定铜锌合金中铜的质量分数。主要实验步骤如下(必要的固定装置已略去):
|
②连接装置并检查装置气密性;
③记录C中液面刻度(C为带有刻度的玻璃管);
④加入药品和水;
⑤待B中不再有气体产生并恢复至室温后,记录C中液
面刻度,计算得到气体的体积为V mL(经查,该气体密度为ρg/L);
(1)正确的操作顺序是 ;
(2)该合金中锌的质量分数为 %,(用W、V、ρ表示)
实验后,小明思考,想到了以下内容:
(3)他认为若在实验前将块状的铜锌合金磨成粉末状,实验效果更好,原因在于 ;
(4)还可通过测定充分反应后试管B中的固体质量来达到实验目的。若按这种方法,除图中的仪器外,还需用到的玻璃仪器有烧杯、 、玻璃棒等。
(1)下列说法错误或实验数据不合理的是 (填序号);
①将实验剩余的药品放回原试剂瓶;
②实验室用高锰酸钾制氧气,在试管口附近放一团疏松的棉花;
③滴瓶上的滴管使用后,应及时清洗干净;
④烧杯可以直接在酒精灯火焰上加热;
⑤加热时,试管中的液体不能超过试管容积的1/3;
⑥实验室用CO与 Fe2O3反应制取铁时,先通CO,再点燃酒精灯;
⑦用托盘天平称取15.65gNaCl固体;
|
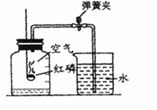
(2)(2分)右图装置的实验目的是 ;
整个实验过程中观察到的现象是
;
(3)(2分)下列实验设计与对应的实验目的表述不一致是 (填序号)。



①探究水的组成 ②证明黄铜与纯铜的抗腐蚀强弱 ③检验氢气的纯度
| |
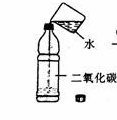


④证明二氧化碳与水反应 ⑤证明一氧化碳具有还原性和可燃性 ⑥探究分子的运动
|


⑦探究二氧化碳的密度比空气大 ⑧探究燃烧的条件