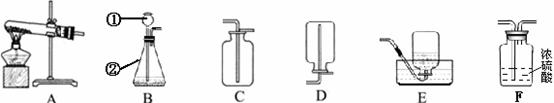
某探究小组同学研究金属铝与稀盐酸的反应速率受外界因素影响的情况。
实验药品:5%盐酸、10%盐酸、质量相同的铝片和铝粉(金属表面氧化膜都已除去);每次实验各种酸的用量均为50. 0mL,金属用量均为9. 0g。
(1)写出铝与盐酸反应的化学方程式 。
(2)该小组设计了如下影响反应速率因素的实验(温度控制为25℃和35℃)。请你根据实验目的帮助该小组完成以下实验设计表(用量:酸均为50. 0mL、铝为9. 0g过量):
| 实验目的 | 实验 编号 | 温度 | 金属铝 形态 | 盐酸浓度 |
| 1. 实验①和②探究盐酸浓度对该反应速率的影响; 2. 实验①和③探究温度对该反应速率的影响; 3. 实验①和④探究金属颗粒大小(铝片、铝粉)对该反应速率的影响。 | ① | 25˚C | 铝片 | 10% |
| ② | ||||
| ③ | ||||
| ④ |
(3)根据实验①和③得到的结论是_______________________________________________。
某氢化物是汽车的清洁燃料,常温常压下是气态,在微微加压时变为液体,可储存在钢瓶中,为汽车供油。
 |
(1)根据表中的几种碳氢化合物的沸点判断,
最适合做汽车清洁燃料的物质是 ,这种燃料在汽化时会从周围 (选“吸收”、“放出”)热量。
(2)该物质在汽缸内燃烧所需要的条件是_____、_____,充分燃烧后的产物是 。
下表是某同学用多种方法鉴别物质的情况,其中两种方法都正确的是
| 选项 | 需要鉴别的物质 | 方法和所加试剂 | |
| 方法一 | 方法二 | ||
| A | 稀盐酸和氢氧化钠溶液 | 用pH试纸检验 | 加入硫酸铜溶液 |
| B | 碳酸钙和硫酸钡 | 加入足量水 | 加入盐酸 |
| C | 稀盐酸和稀硫酸 | 滴加氯化钡溶液 | 滴加紫色石蕊溶液 |
| D | 硝酸铵和硫酸钾 | 加氢氧化钙研磨 | 加入适量水观察是否溶解 |