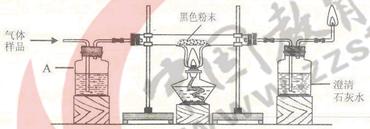
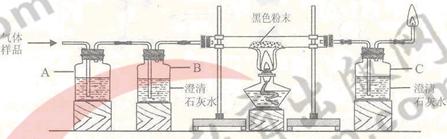
用作牙膏摩擦剂的轻质碳酸钙可以用矿石A来制备,某化学兴趣小组设计了2种转化流程,如下图所示。

已知:a.二氧化碳持续通入氢氧化钙溶液发生如下反应:
|
b.碳酸氢钙微溶于水,微热易分解: Ca(HCO3)2===== CaCO3↓+H2O+ CO2↑;
c.生石灰与水充分反应后可得到颗粒非常细小的熟石灰浆。
试填空。
(1) 小王主张用流程①、②、④和操作Ⅱ的设计,认为其工艺简单。查阅资料④的化学反应原理为: Na2CO3+Ca(OH)2→CaCO3↓+2NaOH。
反应①的化学方程 ;反应类型为 反应;
操作Ⅱ包括 等工序。
(2)制轻质碳酸钙时,D为 (选填“悬浊液”或“溶液”或“乳浊液”),
理由是: 。
(2) 小李认为流程①、②、③和操作I比小王的主张更好,其理由是:
(3) _______________
;操作I包括搅拌和微热等工序。
木炭在氧气中燃烧比在空气中燃烧得更旺;夏天,将食品放在冰箱里不容易腐烂。说明反应物的浓度和温度对化学反应快慢(反应速率)有影响。那么,浓度和温度是如何影响化学反应速率的?
设计方案:同学们利用双氧水和二氧化锰反应来探究上述问题,设计了下列3组实验。其中二氧化锰的作用是 。
| 组别 | 温度 | 二氧化锰的质量 | 双氧水的浓度和体积 | 观察产生气泡的速率 |
| 1 | 室温 | 0.5g | 5%、50 mL | 反应平稳,有大量气泡产生 |
| 2 | 加热 | 0.5g | 5%、50 mL | 气泡急速产生,并产生大量白雾 |
| 3 | 室温 | 0.5g | 30%、50 mL | 气泡呈爆发式产生,并带出反应液 |
分析探究:哪两组实验用来探究浓度对化学反应速率的影响? 。
通过上述实验得出的结论是:
① 、
② 。
讨论反思:通过三组实验的观察与比较,你认为第 组方案比较适合在实验室制取氧气。写出发生反应的化学方程式 。
某同学进行中和反应实验:取适量氢氧化钠溶液于烧杯中,滴加几滴紫色石蕊
溶液,然后逐渐滴入稀盐酸,测得溶液的pH及颜色变化情况如下表。
| 滴入盐酸的体积/mL | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| pH | 13.0 | 12.8 | 12.5 | 12.2 | 7.0 | 2.0 | 1.7 | 1.6 |
| 溶液颜色 | 红色 | 紫色 | 红色 | |||||
(1) 从上表中获得的信息有:紫色石蕊溶液遇碱变蓝色,遇酸变红色。请任意再写两点。
① 。
② 。
(2) 加入紫色石蕊的目的是 。
当加入7 mL稀硫酸时,溶液中的溶质为 。