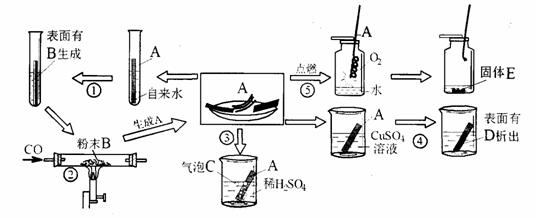
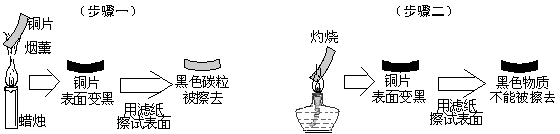某化学活动小组用化学方法测定一种钢样品中铁的含量。同学们称取了5.7g钢样品,投入装有50.0g稀硫酸(足量)的烧杯中(烧杯质量也为50.0g,样品中杂质不与酸反应)。在实验过程中对烧杯(包括溶液和残余固体)进行了四次称量,记录如下表:
| 反应时间 | t0 | t 1 | t 2 | t 3 |
| 烧杯和药品质量/g | 105.7 | 105.6 | 105.5 | 105.5 |
(1)反应中产生氢气 ▲ g;
(2)这种钢样品中铁的质量分数是多少?(写出计算过程,精确到0.1%)▲
(3)有同学提出:在氧气中灼烧钢样品可使碳变为二氧化碳气体逸出,灼烧后钢样品质量会减轻。可是他们将一定量的钢样品灼烧后,发现质量反而增加了许多。原因是 ▲ 。
以下是某实验小组在探究金属化学性质过程中的部分实验记录,请你根据实验记录回答下列问题:
大小、形状都相同的金属与完全相同的稀盐酸反应的记录如下
| 金属 | 铝片 | 锌片 | 铁片 | 铜片 | 银片 |
| 反应现象 | 开始无气泡,过一段时间后缓慢出现气泡 | 产生气泡且速度较快 | 产生气泡但速度缓慢 | 无气泡 | 无气泡 |
(1)根据金属活动性顺序和以上记录可知,能与稀盐酸反应的金属应具备的条件是:
▲ 。
(2)根据金属活动性顺序,铝片应比锌片活泼。但实验记录中铝与稀盐酸的反应速度比锌的更 ▲ (填“快”或“慢”)。你认为上述实验记录中出现与金属活动性顺序相违背的现象的原因是 ▲ 。
(3)在该实验探究的过程中,实验小组因故没有完成铜与银的金属活动性强弱的比较。下列哪组反应能发生并能完成以上比较实验:
A、铜片与AgNO3溶液 ;B、银片与Cu(NO3)2溶液;C、铜片与盐酸D、银片与盐酸。
你所选用的一组试剂是 ▲ (填编号)。
相应反应的化学方程式是: ▲ 。
下表是几种可燃物在压强为101KPa时间的沸点。请你回答:
| 可燃物 | 甲烷CH4 | 乙烷X | 丙烷C3H8 | 丁烷C4H10 | 戊烷C5H12 |
| 沸点/℃ | —164 | —88.6 | —42.1 | —0.5 | 36.1 |
(1) “祥云”火炬中的燃料含有C3H8,它燃烧的化学方程式是 ▲ ;
(2) 乙烷(X)的化学式是 ▲ ;
(3)打火机的燃料稍加压即可以液化,减压后(打开开关)液体又容易气化,遇明火即燃烧。上表中可做打火机燃料的是 ▲ ;
(4)请你依表中所给信息总结出一条有关结构和性质之间的规律 ▲ 。