某水泥厂化验室,为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水。)有关实验数据如下表:
| 反应前 | 反应后 | ||
| 实验 数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 150 g | 12 g | 163.4 g | |
(1)根据质量守恒定律可知,反应中生成二氧化碳的质量为 g。
(2)求该石灰石中碳酸钙的质量分数。(要有计算过程)
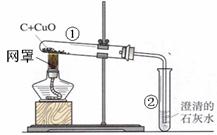
(1)铁是一种最主要的金属材料,实验室里用一氧化碳还原氧化铁得到铁,实验过程中,先插入一氧化碳的目的是 。
(2)炼铁厂常以焦炭、赤铁矿、空气为主要原料炼铁,反应过程如下:
![]()
![]()
|
|
① ② ③
写出②③两部的化学方程式 、 。
(3)生产上用1000t含80%氧化铁的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是 t。(保留整数)
下表是某同学探究金属活动性顺序的实验报告,请你在空白处填空。
| 实验步骤 | 实验现象 | 解释 |
| (1)将锌片、铜片分别投入到盛有稀H2SO4的试管中。 |
| 反应的化学方程式为
|
| (2)将铜片投入到盛有AgNO3溶液的试管中。 | 在铜片的表面覆盖了一层银白色物质,溶液呈 色 | 反应的化学方程式为
|
| 结论|:Zn、Cu、Ag三种金属由强到弱的活动顺序为 | ||
下表是元素周期表的一部分:
|
周期 | IA | 0 | ||||||
| 一 | 1 H 1.008 | ⅡA | ⅢA | ⅣA | V A | ⅥA | ⅦA | 2 He 4.003 |
| 二 | 3 Li 6.941 | 4 Be 9.012 | 5 B 10.8l | 6 C 12.01 | 7 N 14.0l | 8 O 16.00 | 9 F 19.00 | 10 Ne 20.18 |
| 三 | 11 Na 22.99 | 12 Mg 24.31 | 13 Al 26.98 | 14 Si 28.09 | 15 P 30.97 | 16 S 32.06 | 17 Cl 35.45 | 18 Ar 39.95 |
(1)12号元素的元素符号为 ;Be元素的相对原子质量为 。
(2)相对原子质量为22.99的元素属 (填“金属”或“非金属”);Ne的化学性质_______。
(3)表中不同种元素最本质的区别是 (填字母)。
A.质子数不同 B.相对原子质量不同 C.中子数不同
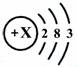
(4)为某元素的原子结构示意图,该元素位于周期表中第 周期。
 (1)用A和C组合装置制取氧气,发生反应的化学方程式为_________________ ___ __,
(1)用A和C组合装置制取氧气,发生反应的化学方程式为_________________ ___ __,

 族
族