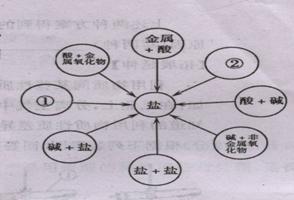
根据下列装置图.回答有关问题:
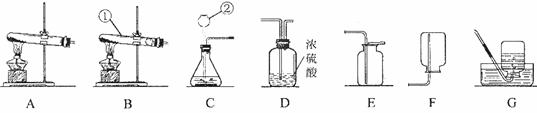
(1)写出装置中标号仪器的名称:① ;② 。
(2)实验室用高锰酸钾制取氧气,可选用的发生装置是 (填字母)。
(3)写出实验室制取二氧化碳的化学方程式 ,该反应
属于 反应(填基本反应类型)根据上图组装一套制取干燥CO2的装置 (用字母表示),验满的方法是 。
(4)某化学探究小组用盐酸与大理石反应研究影响反应剧烈程度的因素。实验温度为25℃、35℃;大理石有细颗粒与粗颗粒两种规格,每次实验取用含碳酸钙60%的大理石10 g;所用盐酸的质量分数为9.125%、18.25%,每次实验盐酸的用量为20mL(假设9.125%、18.25%的盐酸的密度均为1 g/cm3;大理石中杂质不与盐酸反应)。
①提出假设:盐酸与大理石反应的剧烈程度与所用盐酸的质量分数、大理石规格、反应温度有关。
②实验设计与实施:完成以下实验设计方案并实验。
| 实验 编号 | T/℃ | 大理石 规格 | 盐酸的 质量分数 | 完全反应 的时间/s | 实验目的 |
| a | 25 | 粗颗粒 | 18.25% | 160 | (I)实验a和b探究同体积下盐酸质量分数对该反应剧烈程度的影响。 (II)实验a和c探究温度对该反应剧烈程度的影响。 (Ⅲ)实验a和d探究大理石规格对该反应剧烈程度的影响。 |
| b | 210 | ||||
| c | 35 | 粗颗粒 | 18.25% | 60 | |
| d | 100 |
③实验结论: 。
某学习小组将“从空气中制取氮气”作为研究课题,以下是他们的实验方案:
(1)写出图1装置 A中发生反应的化学方程式 ,装置B的作用是 ,
装置C的作用是. 。
方案二:
(2)甲、乙两位同学分别收集一瓶装置图1的装置B中放出的气体,用图2装置进行实验,其中甲同学选用红磷,乙同学选用木炭。你认为:选用 (填“红磷”或“木炭”)的方法不科学,原因是 ;
(3)分析误差:此法得到的氮气密度与氮气的实际密度有误差,请你分析产生误差的可能原因(写两种) 、 ;
(4)利用物质间某些性质的差异选用不同的方法将它们分离,是分离物质的基本思路。例如:在工业上,分离空气中的氮气和氧气是利用它们 的不同。请列举一种你所知道的利用物质性质差异分离物质的方法 。
![]()

下表列出了除去物质中所含少量杂质的方法,其中错误的是 ( )
| 物质 | 所含杂质 | 除去杂质的方法 | |
| A | CO | CO2 | 通过足量氢氧化钠溶液,干燥 |
| B | NaCl | 泥沙 | 溶解、过滤、蒸发 |
| C | NaOH溶液 | Na2CO3 | 加入足量稀盐酸至不再产生气泡 |
| D | Cu(NO3)2溶液 | AgNO3 | 加入过量的铜粉,过滤 |