氢氧化钠是一种重要的化工原料,也是实验室中常见的化学药品。
【观察】(1)实验室中盛放氢氧化钠溶液的试剂瓶是 (a、细口瓶;b、广口瓶),瓶塞是 (a、橡皮塞;b、玻璃塞)。
(2)盛放氢氧化钠溶液的试剂瓶的瓶口有白色固体。
【解释】形成白色固体的原因是: 。
【问题】白色固体中含有哪些物质?
【资料】(1)NaOH和 Na2CO3 受热不分解;
(2)NaOH的熔点为318.4℃,沸点为1390℃;Na2CO3的熔点为851℃。
【设计与实验】(请你帮助甲、丙实验小组完成实验报告)
实验小组甲:
| 实验过程与数据 | 分析与结论 |
| (1)取3g白色固体,加热 (2)冷却后称得固体的质量为2.9g | 白色固体中含有 |
实验小组乙:
| 实验步骤 与现象 | 分析与结论 |
| (1)取少量样品,溶于水中 (2)滴入澄清的石灰水产生白色沉淀,继续滴加至不再产生白色沉淀为止,过滤 (3)在滤液中加入无色酚酞,溶液显红色 | 原白色固体中 一定含有NaOH和 Na2CO3 |
实验小组丙:
| 实验步骤 | 实验现象 | 分析与结论 |
| (1)取少量样品,溶于水 (2)滴入CaCl2溶液 (3)
(4) |
| 原白色固体中一定含有 Na2CO3,一定不含NaOH |
【交流与评价】
三个实验小组代表汇报了各自的实验及其结论后,老师肯定了小组甲和小组丙的实验探究,同时指出了实验小组乙中存在的错误。这个错误是: 。
【拓展】老师提供了一个可证明原白色固体中成分的探究示例:
实验过程与数据:
步骤1:收集瓶口处白色固体,加热 ;
步骤2:取该白色固体样品3g;
步骤3:将固体溶于水后,滴入稀盐酸到不再产生气泡;
步骤4:测出收集到气体的质量为1.1g
二.计算分析与结论:
①计算分析:
②结论:原白色固体的成分为
某节化学实验课上,同学们要完成某实验,老师已在实验台前准备了如下仪器和药品:
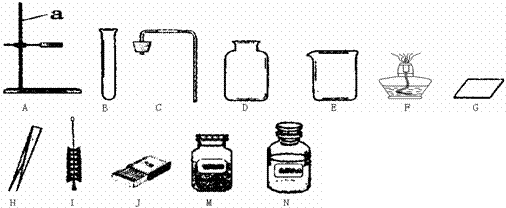 |
请回答:
(1) 指出上图中仪器a的名称:
(2) 操作 以下是甲同学完成该实验主要操作过程的示意图。按评分标准,每项操作正确得1分,满分5分,实验完毕后甲得了3分。请找出他失分的操作并说明原因:
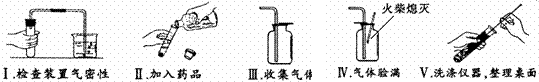 、 ;
、 ;
分析 你认为甲同学制取了 气体。乙同学还利用右图装置测定生成的该气体的体积,其中在水面上放一层植物油目的是 。
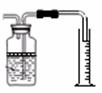
(3) 丁同学利用加热草酸晶体的方法来获得CO ,草酸晶体熔点低,加热会熔化、汽化和分解。其化学方程式为: H2C2O4 ![]() CO2↑+ H2O + CO↑;发生装置应选 (填仪器的字母),能否选用加热草酸晶体用于实验室制取CO?理由是 。
CO2↑+ H2O + CO↑;发生装置应选 (填仪器的字母),能否选用加热草酸晶体用于实验室制取CO?理由是 。
