溶液与人类生活息息相关,溶液的配制是日常生活和化学实验中的常见操作。
下表是硫酸溶液和氨水的密度与其溶质的质量分数对照表(20℃)
请分析下表后回答下列问题
| 溶液中溶质质量分数/% | 4 | 12 | 16 | 24 | 28 |
| 硫酸溶液的密度/g/mL | 1.02 | 1.08 | 1.11 | 1.17 | 1.20 |
| 氨水的密度/ g/mL | 0.98 | 0.95 | 0.94 | 0.91 | 0.90 |
(1)20℃时,随着溶液中溶质的质量分数逐渐增大,硫酸溶液的密度逐渐 (填“增大”“减小”或“不变”,下同),氨水的密度 .
(2)取12%的硫酸溶液100g配制成6%的溶液,向100g12%的硫酸溶液中加水的质量应
100g(填“大于”、“小于”或“等于”)
根据溶解度曲线回答问题
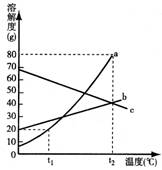 |
(1)溶解度随温度升高而增大的物质是
(2)t2℃时,溶解度相等的是
(3)t2℃时,100g水中加入20ga物质,溶液不饱和,
为使其饱和,可再加入a物质 g,或使
其温度降到 ℃
