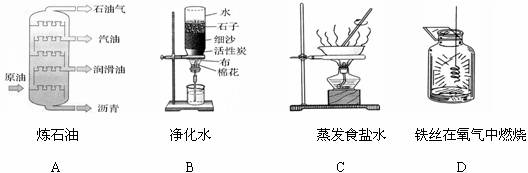
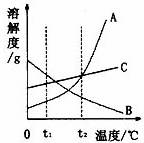
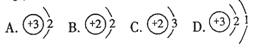下列关于化学实验的“目的一操作一现象一结论”的描述正确的是( )
| 实验过程 组别 | 实验目的 | 所加试剂 (或操作) | 实验现象 | 实验结论 |
| A | 检验某混合气体中是否含有CO2气体 | 通入澄清 石灰水中 | 无明显现象 | 该气体中不含CO2 |
| B | 除去KCl中的 少量K2CO3 | 稀盐酸 | 有气泡产生 | K2CO3已被除完 |
| C | 区分硬水和蒸馏水 | 肥皂水 | 产生大量泡沫 | 该液体为蒸馏水 |
| D | 用排空气法收集CO2时检验集气瓶中CO2是否集满 | 将燃烧的木条伸入瓶内 | 木条熄灭 | 瓶内CO2已集满 |
小东从海边捡来一些嵌有沙砾的贝壳(主要成分为碳酸钙),为测定碳酸钙的含量,他做了如下实验:首先称取50 g贝壳样品,然后将150 mL的盐酸分5次加入(假设其余杂质均不与盐酸反应)。实验过程中的数据记录如下:
| 稀盐酸 | 第一次30 mL | 第二次30 mL | 第三次30 mL | 第四次30 mL | 第五次30 mL |
| 剩余固 | 40.0 g | X | 20.0 g | 10.0 g | 5.0 g |
(1)X = g;
(2)小东测得贝壳样品中碳酸钙的质量分数是 ;
(3)若把二氧化碳收集起来,共有多少g?
“用双氧水和二氧化锰制氧气”的反应方程式为: 。
某同学做了该实验后,展开了下列思考与探究:
(1)催化剂MnO2的用量对反应速率有没有影响呢?
他做了这样一组实验:每次均用30 mL 10%的H2O2溶液,采用不同量MnO2粉末做催化剂,测定各次收集到500 mL氧气时所用的时间,结果如下:(其他实验条件均相同)
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| MnO2粉末用量/g | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 | 1.0 |
| 所用时间/s | 17 | 8 | 7 | 5 | 4 | 3 | 2 | 2 | 2 | 2 |
请分析表中数据回答:MnO2的用量对反应速率有没有影响呢?如果有,是怎样影响的呢?
(2)H2O2溶液的溶质质量分数对反应速率有没有影响呢?
他又做了一组实验:每次均取5 mL 30%的H2O2溶液,然后稀释成不同溶质质量分数的溶液进行实验。记录数据如下:(实验均在20 ℃室温下进行,其他实验条件也均相同)
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| H2O2溶液溶质质量分数 | 1% | 3% | 5% | 10% | 15% | 20% | 25% | 30% |
| MnO2粉末用量(克) | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 |
| 收集到540 mL气体时所用时间/s | 660 | 220 | 205 | 80 | 25 | 9 | 4 | 3 |
| 反应后液体温度/℃ | 24 | 34 | 39 | 56 | 65 | 67 | 69 | 70 |
请分析表中数据回答:H2O2溶液的溶质质量分数对反应速率有没有影响呢?如果有,是怎样影响的呢?
由表中数据还可看出,该反应是个 反应(填“放热”或“吸热”)。
(3)还有哪些因素可能影响该反应的速率呢?
请说出你的一个猜想: 。