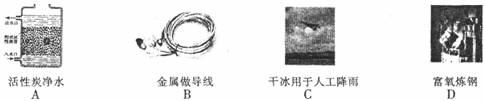
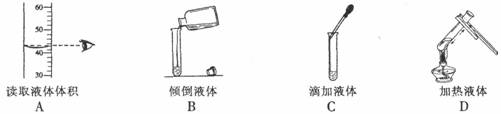
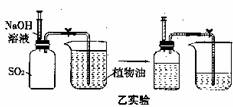
0 44870 44878 44884 44888 44894 44896 44900 44906 44908 44914 44920 44924 44926 44930 44936 44938 44944 44948 44950 44954 44956 44960 44962 44964 44965 44966 44968 44969 44970 44972 44974 44978 44980 44984 44986 44990 44996 44998 45004 45008 45010 45014 45020 45026 45028 45034 45038 45040 45046 45050 45056 45064 211419