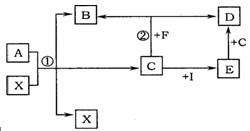
某研究性小组设计了下表中的三组实验,分别向甲物质中逐滴加入相应的乙溶液至过量。
| ① | ② | ③ | |
| 田 | 铜、锌的混合物 | 硫酸和硫酸铜的混合溶液 | 盐酸和氯化铵的浓溶液 |
| 乙 | 稀硫酸 | 氢氧化钠溶液 | 氢氧化钠浓溶液 |
反应过程中生成气体或沉淀的质量与加入乙的质量关系,能用如图所示曲线表示的是 ( )

A.①② B.①③ C.②③ D.①②③
为得到纯净的物质,某同学设计下表中的除杂方法,其中方法正确的是 ( )
| 物质 | 所含杂质 | 除去杂质的方法 | |
| A | NaCl溶液 | Na2CO3 | 加人稀硫酸至不再产生气泡 |
| B | CuO粉末 | C | 加入过量稀盐酸,充分反应 |
| C | N2气体 | O2 | 将气体缓缓通过灼热的铜网 |
| D | KCl溶液 | CuCl2 | 加入氢氧化钠溶液至不再产生沉淀 |