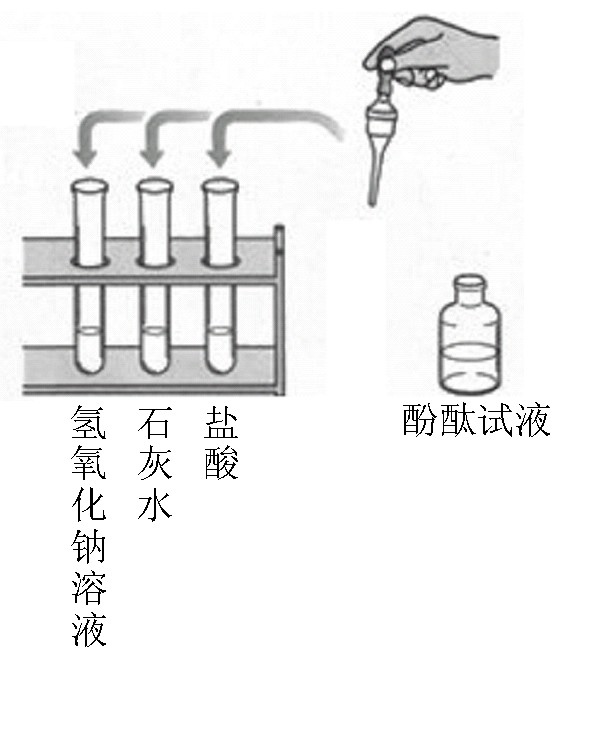
小明在学习酸的性质时,用大小、外形均相同的铝片分别与等浓度的稀盐酸、稀硫酸反应,他意外发现:铝片与稀盐酸反应放出气泡的速度明显快于稀硫酸。是什么导致了反应现象的差异呢?
(1)小明从微观角度得出,H+浓度相同的盐酸、硫酸中,只是所含 不同。
于是小明提出了如下猜想:
①Cl━ 能促进铝和盐酸的反应,SO42━ 对反应无影响;
②Cl━ 对反应无影响,SO42━ 能抑制铝和盐酸的反应;
③Cl━ 能促进铝和盐酸的反应,SO42━ 能抑制铝和盐酸的反应。
为验证猜想,他进行了如下实验探究。针对探究过程回答问题:
组别 | 相同的铝片 | H+浓度相同的酸 | 反应片刻后加入少量试剂 | 加入试剂后的反应现象 | 结论 |
一 | 1g铝片 | 5ml盐酸 | Na2SO4 | 无明显变化 | 和 离子对反应无影响 |
二 | 1g铝片 | 5ml硫酸 | NaCl | 明显加快 | 离子对反应有促进作用 |
(2)请将表格中空格补充完整。
(3)上述猜想 是成立的。
(4)若将第二组实验中添加的试剂NaCl改为盐酸,能否完成探究任务? ,
原因是 。
归纳与演绎是重要的科学方法,也是常用的化学学习方法。
(1)某研究小组对用双氧水分解生成水和氧气的实验条件进行探究,完成了以下实验:
①往盛有5 ml 5%H2O2溶液的试管中,伸入带火星的木条,木条不复燃。
②往盛有5 ml w% H2O2溶液的试管中,加入a g MnO2,伸入带火星的木条,木条复燃。
③往盛有5 ml w% H2O2溶液的试管中,加入a g Fe2O3,伸入带火星的木条,木条复燃。
④经检验,②③中反应后试管中仍分别含有a gMnO2和 ag Fe2O3
问题一:请你写出用双氧水和二氧化锰制氧气的化学反应方程式
问题二:MnO2和 Fe2O3在上述反应中的作用是 ;实验②③中的H2O2的浓度(w%)以 为宜。
(2)研究小组还对溶液浓度、催化剂的种类等实验条件进行探究。下表选取了部分实验数据:用足量等体积H2O2溶液制取相同体积O2所需要的时间
浓度 时间(min) 条件 | 30%H2O2 | 15%H2O2 | 5%H2O2 |
a g MnO2 | 0.2 | 0.8 | 2.0 |
ag Fe2O3 | 0.7 | 9.0 | 16.0 |
问题三:从上表中能得到哪些结论?(写出一条结论)
填写下列表格:
(1) | (2) | |||||
化学符号 | H | 2P2O5 | Al3+ | |||
名称或意义(只写一种) | 2个铁原子 | 由3个氧原子构成的一个臭氧分子 | 一氧化碳中碳元素显+2价 | |||
某中学九年级A、B两班同学做常见酸和碱与指示剂反应的实验,使用的试剂如右图所验后废液分别集中到废液缸中。某研究小组对此废液进行了检测,结果如下:
废液来源 | 检测方法和结果 |
A班 | 观察废液呈无色 |
B班 | 观察废液呈红色 |
请你根据实验现象判断,对该废液的成分的说法错误的是( )
A.A班废液中一定含有的物质只有氯化钠
B.A班废液中可能含有盐酸
C.B班废液的成分中肯定没有盐酸
D..B班废液中可能含有氢氧化钠