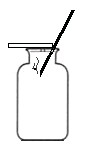
下图是实验室常用来制取气体的装置,根据所学的知识回答以下问题:
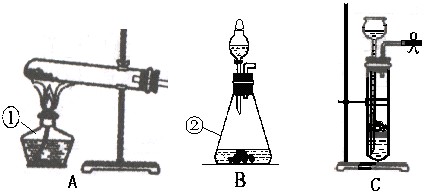
(1)标号仪器的名称:
① ②
(2)实验室用过氧化氢溶液制取氧气,选用的最佳装置是 (填装置序号);反应的化学方程式是: 。
(3)某同学为了探究H2O2溶液的质量分数对反应速率有没有影响做了一组实验:每次均取5ml30%的H2O2溶液,然后稀释成不同溶质质量分数的溶液进行实验。记录数据如下:
实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
H2O2溶液溶质质量分数 | 1% | 3% | 5% | 10% | 15% | 20% | 25% | 30% |
MnO2粉末用量(克) | m | m | m | m | 0.6 | 0.6 | 0.6 | 0.6 |
收集到500ml气体所需时间(秒) | 660 | 220 | 205 | 80 | 25 | 9 | 4 | 3 |
反应后液体温度(℃) | 24 | 34 | 39 | 56 | 65 | 67 | 69 | 70 |
①该实验的目的是 ;
m的数值为 g。
②由表中数据观察:H2O2溶液的质量分数对反应速率有没有影响呢?如果有,是怎样影响呢? ;该反应是一个 反应(填“放热”或“吸热”)。
(4)13.6g溶质质量分数为10%的过氧化氢溶液中含有H2O2的质量是 g;该过氧化氢完全分解,可得氧气的质量是 g 。
某化学兴趣组的同学想通过实验测定雨水的pH,使用pH试纸测定溶液pH的具体操作是: 。 另一兴趣小组的同学取刚降到地面的雨水水样,用pH计每隔几分钟测一次pH,其数据如下表所示:
测定时刻 | 5:05 | 5:10 | 5:15 | 5:20 | 5:25 |
pH | 4.95 | 4.94 | 4.88 | 4.86 | 4.85 |
根据表中数据分析:
(1)所得雨水 (填“是”、“不是”)酸雨;在测定期间内,雨水样品的酸性 (填“增强”或“减弱”)。
(2)经调查,该地区附近有较集中的工厂,这些工厂和周围的群众使用的燃料主要是煤。试分析造成酸雨的主要原因: (用化学方程式表示)。
下面是三种固体在不同温度下的溶解度。
温度/℃ | 0 | 20 | 40 | 60 | 80 | |
溶 解 度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | |
NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | |
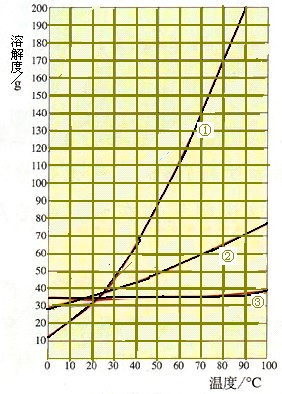
某课外小组同学根据上表数据绘制出溶解度曲线图如下图。
(1)硝酸钾的溶解度曲线是 (填序号);由图中可知这三种物质的溶解度随 升高而 。
(2)20℃时,将40g氯化钠固体投入100水中,充分溶解后可得氯化钠饱和溶液 g。
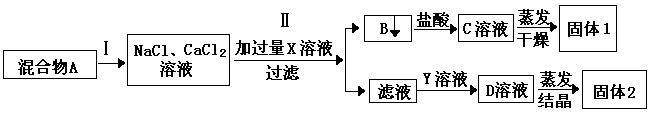
(3)某同学欲从含有少量氯化钠的硝酸钾中分离出硝酸钾,他应采取的方法是 。
现有a、b、c、d四种无色溶液,分别是碳酸钠溶液、稀硫酸、氯化钡溶液、盐酸中的一种。根据表格中它们两两间相互反应的实验记录,推断a、b、c、d的顺序正确的是
a | b | c | d | |
b | 无明显现象 | —— | 有气体生成 | 有沉淀生成 |
c | 有气体生成 | 有气体生成 | —— | 有沉淀生成 |
A、H2SO4、HCl、Na2CO3、BaCl2 B、HCl、H2SO4、Na2CO3、BaCl2
C、Na2CO3、H2SO4、HCl、BaCl2 D、HCl、Na2CO3、H2SO4、BaCl2
下列实验的现象和结论不合理的是
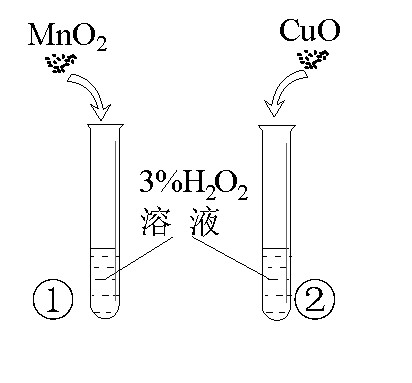
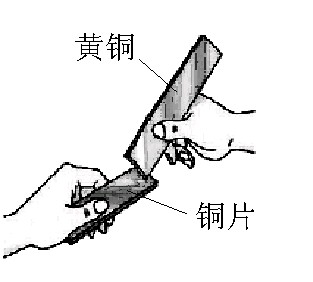
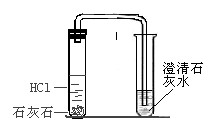
项目 | A.比较催化效果 | B.比较硬度 | C.检验碳酸根 | D.验证CO2 |
实验 |
|
|
|
|
现象和 结论 | ①试管比②试管放出气泡快 — MnO2比CuO的催化效果好 | 铜片上有划痕 —黄铜的硬度比铜大 | 有无色气泡生成,石灰水变浑浊 — 碳酸盐能与HCl反应生成CO2 | 木条熄灭 — CO2不支持燃烧 |