0 43428 43436 43442 43446 43452 43454 43458 43464 43466 43472 43478 43482 43484 43488 43494 43496 43502 43506 43508 43512 43514 43518 43520 43522 43523 43524 43526 43527 43528 43530 43532 43536 43538 43542 43544 43548 43554 43556 43562 43566 43568 43572 43578 43584 43586 43592 43596 43598 43604 43608 43614 43622 211419
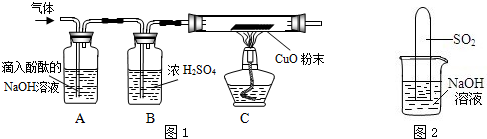
 某化学兴趣小组同学对“制镁企业不能使用CO2灭火器作为消防器材”的问题进行探究,请你参与他们的活动.
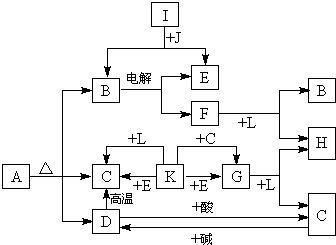
某化学兴趣小组同学对“制镁企业不能使用CO2灭火器作为消防器材”的问题进行探究,请你参与他们的活动.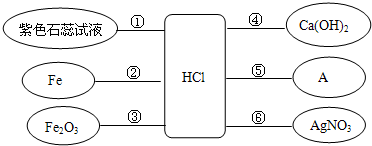 归纳与整理是学习的常用方法.某同学对盐酸的性质进行了如下所示的归纳与整理,“”表示物质两两之间能发生化学反应.请回答下列问题:
归纳与整理是学习的常用方法.某同学对盐酸的性质进行了如下所示的归纳与整理,“”表示物质两两之间能发生化学反应.请回答下列问题: