0 42885 42893 42899 42903 42909 42911 42915 42921 42923 42929 42935 42939 42941 42945 42951 42953 42959 42963 42965 42969 42971 42975 42977 42979 42980 42981 42983 42984 42985 42987 42989 42993 42995 42999 43001 43005 43011 43013 43019 43023 43025 43029 43035 43041 43043 43049 43053 43055 43061 43065 43071 43079 211419
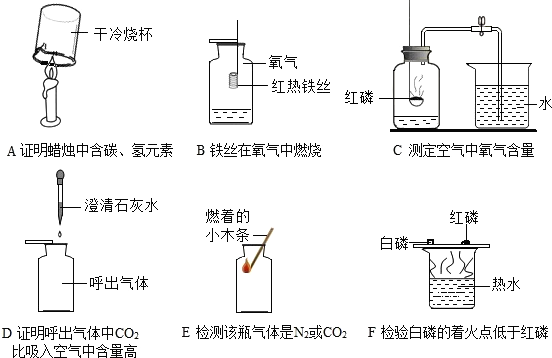
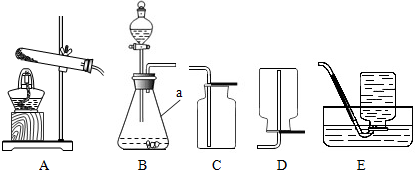
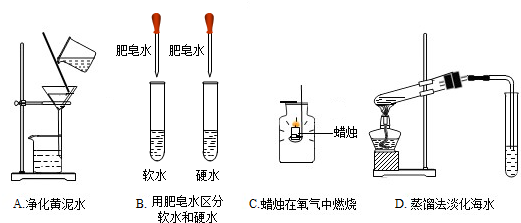
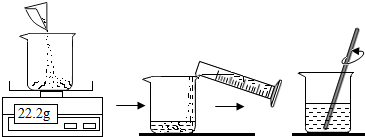
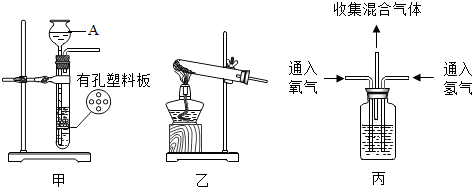
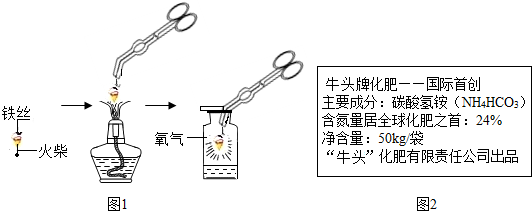
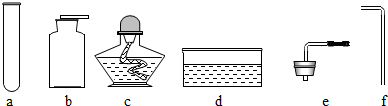
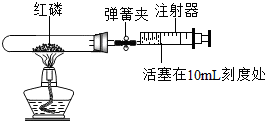
 某化学兴趣小组的同学对空气中氧气含量的测定实验进行探究.
某化学兴趣小组的同学对空气中氧气含量的测定实验进行探究.