某煤厂向原煤中加入适量熟石灰制成“环保煤”,以减少二氧化硫造成的空气污染.该环保煤燃烧时与SO2反应的化学方程式为2Ca(OH)2+2SO2+O2
2X+2H2O,则X的化学式为( )
| ||
| A、CaSO4 |
| B、CaS |
| C、CaSO3 |
| D、Ca(HSO4)2 |
在化学反应前后,下列各项中肯定没有发生变化的是( )
①原子数目 ②分子数目 ③元素种类 ④原子的种类 ⑤物质种类 ⑥物质的总质量.
①原子数目 ②分子数目 ③元素种类 ④原子的种类 ⑤物质种类 ⑥物质的总质量.
| A、①②③⑤ | B、①②④⑥ | C、①③④⑥ | D、①③④⑤⑥ |
某一物质在空气中燃烧后,生成H2O和CO2,因此该物质一定含有( )
| A、氧气、氢气和碳 | B、氢气、碳 | C、氧元素、氢元素和碳元素 | D、氢元素和碳元素 |
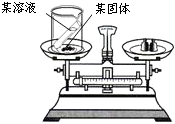 某科学兴趣小组的同学利用如图所示实验装置验证质量守恒定律.下列各种药品组合中,他们应选用( )
某科学兴趣小组的同学利用如图所示实验装置验证质量守恒定律.下列各种药品组合中,他们应选用( )| A、稀盐酸和镁条 | B、稀硫酸和碳酸钠粉末 | C、稀盐酸和铜粉 | D、氯化钙溶液和碳酸钠粉末 |
下列说法中正确的是( )
| A、煤燃烧后剩余的煤渣比较轻,因此不符合质量守恒定律 | B、蜡烛燃烧生成的气态物质的质量之和等于蜡烛减少的质量与消耗的氧气的质量之和 | C、10g的水全部蒸发后生成10g的水蒸气,因此符合质量守恒定律 | D、只要做一个“白磷燃烧前后质量的测定”的实验就能得出质量守恒定律 |
密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:下列说法错误的是( )
|
| A、C一定是化合物,D可能是单质 |
| B、C物质中元素的种类,一定等于A、B、D三种物质中元素的种类 |
| C、反应过程中,物质B与物质D变化的质量比为87:36 |
| D、若物质A与物质C的相对分子质量之比为197:158,则反应中A与C的化学计量数之比为1:2 |
有以下几种说法:在化学反应前后没有发生改变的是:①物质种类;②分子种类;③分子数目;④原子种类;⑤原子数目;⑥原子质量.能正确说明质量守恒定律原因的是( )
| A、① | B、②③ | C、④⑤⑥ | D、①②③④⑤⑥ |
下列说法中能用质量守恒定律解释的是( )
| A、10g酒精和50g水混匀后形成60g酒精溶液 | B、块状红磷被粉碎 | C、1g氢气和8g氧气反应,生成9g水 | D、10g水受热变成10g水蒸气 |
某反应的反应原理为3Cu+8HNO3=3Cu(NO3)2+2X↑+4H2O 则物质X的化学式为( )
| A、NO | B、NO2 | C、N2O5 | D、N2O |
下列说法正确的是( )
| A、跟氧气发生的反应都是氧化反应,所以氧化反应就是物质和氧气发生反应 | B、为了防止热量散失,用酒精灯加热时须用内焰加热 | C、动物的呼吸运动和呼吸作用是不同的,呼吸运动是在膈肌和肋间肌作用下的物理变化而呼吸作用是复杂的化学变化 | D、工业上用分离空气法制取氧气,当把液态空气升温时首先出来的是氧气,因为氧气的沸点是-183℃而氮气沸点为-196℃ |