0 41104 41112 41118 41122 41128 41130 41134 41140 41142 41148 41154 41158 41160 41164 41170 41172 41178 41182 41184 41188 41190 41194 41196 41198 41199 41200 41202 41203 41204 41206 41208 41212 41214 41218 41220 41224 41230 41232 41238 41242 41244 41248 41254 41260 41262 41268 41272 41274 41280 41284 41290 41298 211419
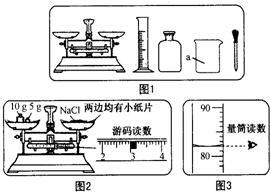 某实验小组利用图1所示仪器进行“配制质量分数一定的氯化钠溶液”的实验:
某实验小组利用图1所示仪器进行“配制质量分数一定的氯化钠溶液”的实验: