下列实验操作中,能达到实验目的的是(____)
选项 | 实验目的 | 实验操作 |
A | 鉴别硬水和软水 | 分别加入肥皂水,振荡 |
B | 证明二氧化碳能与水反应 | 将二氧化碳通入滴有酚酞溶液的水中 |
C | 除去二氧化碳中的一氧化碳 | 点燃 |
D | 验证某瓶气体是二氧化碳 | _________ |
小红按下图装置改进实验,验证了质量守恒定律,还发现产物中有少量黄色固体。
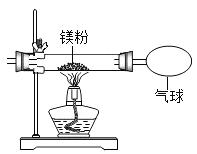
(提出问题)黄色固体是什么?
(查阅资料)①氧化镁为白色固体;
②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
(作出猜想)黄色固体是Mg3N2。
(实验探究)设计实验,验证猜想:
实验操作 | 实验现象及结论 |
__________ | ___________ |
(反思与交流)①空气中N2的含量远大于O2的含量,可是镁条在空气中的燃烧产物MgO却远多于Mg3N2,合理的解释是________。
②同学们又联想到氢气在氯气中能够燃烧,于是对燃烧条件又有了新的认识________。
瑞金市石灰石资源丰富,某课外小组同学为了测定石灰石中碳酸钙的质量分数,取某地石灰石样品9.0g于烧杯中,将50g稀盐酸分5次加入烧杯中,充分反应后(杂质不与稀盐酸反应),测得剩余固体的质量记录如下。
次数 | 1 | 2 | 3 | 4 | 5 |
加入稀盐酸质量/g | 10 | 10 | 10 | 10 | 10 |
剩余固体质量/g | 7.0 | 5.0 | 3.0 | 1.5 | x |
请计算:
(1)x的值为_____。
(2)完全反应后生产二氧化碳的质量为多少?(写出计算过程)______
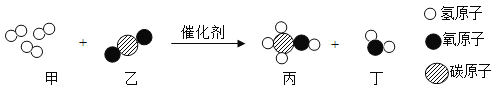
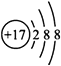 ,该微粒的符号_______________。
,该微粒的符号_______________。

 B.
B.  C.
C.  D.
D. 