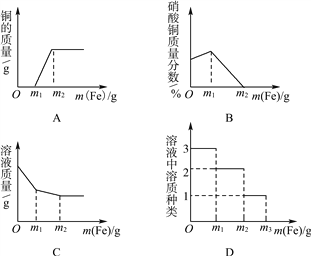
室温下,称取氯化钠和碳酸钠各30g放入同一烧杯中,加入100g水充分搅拌后静置,得到二者的混合溶液.请参照氯化钠、碳酸钠两种物质的溶解度表判断,以下结论不正确的是( )
温度/℃ 溶解度/g 物质 | 0 | 10 | 20 | 30 | 40 |
氯化钠 | 35 | 35.5 | 36 | 36.5 | 37 |
碳酸钠 | 6 | 10 | 18 | 36.5 | 50 |
A. 20℃时,氯化钠的溶解度大于碳酸钠的溶解度
B. 20℃时,未溶解固体是氯化钠和碳酸钠的混合物
C. 30℃时,溶液中氯化钠和碳酸钠的质量分数相同
D. 30℃时,溶液为氯化钠和碳酸钠的不饱和溶液
R是硝酸钾或氯化铵中的一种。硝酸钾和氯化铵的溶解度曲线如图1所示.某化学兴趣小组的同学进行了如图2所示实验。
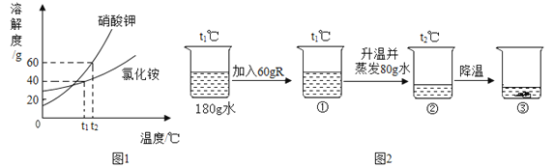
(1)t1℃时,氯化铵的济解度为______g。
(2)①的溶液中溶质质量分数为____________。
(3)根据以上信息可推出R是________(写名称或化学式均可)。
(4)关于图2中烧杯内的物质,以下几种说法正确的有_________。
A.①、②、③中,只有③中上层清液是饱和溶液 |
B.若使③中的固体溶解,可采用加水或升温的方法 |
C.①和②的溶液中,溶质质量相等 |
D.①的溶液中溶质质量分数一定比③的上层清液中溶质质量分数小。 |
合金是由两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质。一般来说,合金的熔点低于任何一种组成金属的熔点。下表是一些金属的熔点数据:
金属 | 铜 | 锌 | 锡 | 铅 | 铋 | 镉 |
熔点/℃ | 1083 | 419.6 | 231.9 | 327.5 | 271.3 | 320.9 |
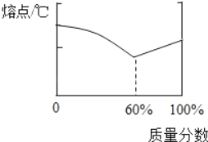
①铅锡合金中某种金属的质量分数与合金的熔点有如图所示的关系,其中横坐标表示的是_____的质量分数;当合金熔点最低时,合金中锡与铅的质量比为_____。
②保险丝由铋、铅、锡、镉组成,其熔点约为_____:
A.15~30℃ B 60~80℃ C 235~250℃ D 300~320℃
兴趣小组的同学对碳酸氢钠、碳酸钠、氢氧化钠的某些性质利用数字化传感器测得烧杯中溶液pH的变化图象进行相关探究。
(提出问题)它们溶液的酸碱性及与酸反应时溶液的pH如何变化?
(实验探究1)向等体积、等浓度的碳酸氢钠、碳酸钠、氢氧化钠溶液中,分别加入几滴紫甘蓝汁液,同时用蒸馏水进行对比实验,观察并记录现象如下:
液体名称 | 蒸馏水 | 碳酸氢钠溶液(A) | 碳酸钠溶液(B) | 氢氧化钠溶液(C) |
紫甘蓝汁液显示的颜色 | 蓝紫色 | 蓝色 | 绿色 | 黄色 |
查阅资料:
pH | 7.5~9 | 10~11.9 | 12~14 |
紫甘蓝汁液显示的颜色 | 蓝色 | 绿色 | 黄色 |
(得出结论1)三种溶液的碱性由强到弱的顺序为______。(用A、B、C表示)
(实验探究2)甲同学在烧杯溶液中加入约5mL稀氢氧化钠溶液,滴入几滴酚酞溶液,此时溶液由 _____色变为____色。向其中加入稀盐酸,该反应的化学方程式为______。
乙同学向一定体积、一定浓度的氢氧化钠溶液中,逐滴加入一定浓度的盐酸,得到pH变化与时间的关系如下图所示.
(得出结论2)①从微观角度分析,该反应的实质是____。
②如图所示,下列说法正确的是(___________)

A.图中c点所示溶液呈碱性
B.图中a点所示溶液中,含有的溶质是只有NaCl
C.该实验是将氢氧化钠溶液逐滴滴入到盛有盐酸的烧杯中
D.由a点到b点的pH变化过程证明酸和碱发生了中和反应