除去下列物质中的杂质(括号内为杂质),完全正确的是
物质 | 选用试剂 | 操作方法 | |
A. | Cu(CuO) | O2 | 通入氧气并加热 |
B. | NaCl(泥沙) | 水 | 溶解、过滤、洗涤、烘干 |
C. | CO2(CO) | ---- | 通氧气并点燃 |
D. | CaCl2溶液(HCl) | 石灰石 | 加入足量石灰石充分反应后,过滤 |
A. A B. B C. C D. D
氧气、二氧化碳是我们身边常见的物质。某兴趣小组对这两种气体研究如下:
Ⅰ.氧气、二氧化碳的制备:
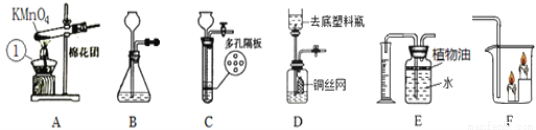
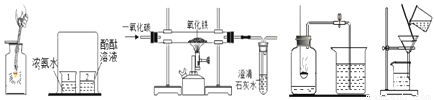
(1)写出A图中有标号仪器①的名称:__________。
(2)写出用KMnO 4制取O 2的化学方程式___________________,该装置中棉花团的作用是__________,图中装置一处明显的错误是__________。
(3)在化学实验室中用石灰石和稀盐酸来制取二氧化碳可选用图B所示的发生装置,该反应的化学方程式是__________。
(4)制二氧化碳也可选用如图C所示的装置,与B装置相比,C装置的优点是_________,用图D装置也可以制取二氧化碳,将石灰石放在铜丝网中,该实验说明了铜____(填“能”或“不能”)和稀盐酸发生反应。
Ⅱ.二氧化碳的性质及氧气的收集研究:
(1)二氧化碳的性质研究
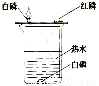
①如图E所示的装置可以测定一段时间收集的二氧化碳的体积,植物油的作用是____。
②如图F所示的装置说明了二氧化碳具有__________的性质,该性质在实际生活中的应用是__________。
③已知:CO 2和SO 2既有相似性,又有差异性。
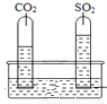
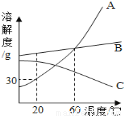
实验一:将收集满两种气体的试管同时倒立于盛水的水槽中,片刻后实验现象如图所示,说明相同条件下SO 2比CO 2__________(填“易”或“难”)溶于水。
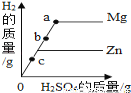
实验二:已知镁条可以在CO 2中剧列燃烧: 2Mg+CO 2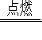 2MgO+C,试推测镁条在SO 2中燃烧的现象为:剧烈燃烧,__________。
2MgO+C,试推测镁条在SO 2中燃烧的现象为:剧烈燃烧,__________。
(2)氧气的收集
(实验1)用向上排空气法收集氧气,当放置在集气瓶口带火星木条复燃时停止收集,测定瓶中氧气的含量,重复实验3次。
(实验2)用向上排空气法收集氧气,当放置在集气瓶口带火星木条复燃后,继续收集40秒,测定瓶中氧气的含量,重复实验3次。
(实验3)用排水法收集氧气,测定瓶中氧气的含量,重复实验3次。
实验数据:
实验1 | 实验2 | 实验3 | |||||||
氧气的体积分数(%) | 79.7 | 79.6 | 79.9 | 88.4 | 89.0 | 87.9 | 90.0 | 89.8 | 89.3 |
氧气的平均体积分数(%) | 79.7 | 88.4 | 89.7 |
数据①由实验1、2可知,用向上排空气法收集氧气时,为提高获得的氧气体积分数,可采取的措施是__________。
②不考虑操作因素,实验3获得的氧气体积分数不能达到100%的主要原因是_________。
铜是生活中常见的一种金属,在生活、生产中有广泛的应用。

(1)如图为铜元素在元素周期表中的信息,铜元素的原子序数为___;
(2)铜离子(Cu2+)的核外电子数为____________;
(3)电气工业上常用铜作电缆的内芯,是利用铜具有良好的_____性;
(4)铜是一种不活泼的金属,但铜制品长期露置在潮湿空气中,表面变绿色,即生成了“铜绿”(化学式:Cu2(OH)2CO3)。
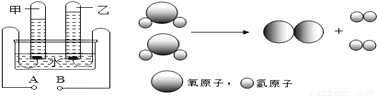
某同学根据铜绿的成分Cu2(OH)2CO3作出猜想:金属铜锈蚀的条件除有氧气和水外,还必须有二氧化碳。为证明“必须有二氧化碳”,需要进行如图所示实验中的_____(选填实验编号甲、乙、丙、丁)

(5)某兴趣小组以锈蚀严重的废铜屑为原料(假设不含其他杂质)制取纯铜。如图是兴趣小组设计的两种回收铜的实验方案:
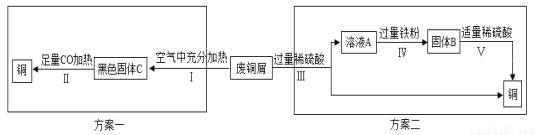
查阅资料:Cu2(OH)2CO3+2H2SO4═2CuSO4+3H2O+CO2↑
(分析评价)
①步骤Ⅲ、Ⅳ、Ⅴ都需要进行的实验操作是___________;
②步骤Ⅳ过程发生反应的化学方程式为__________________、_________________;
③同一份废铜屑分别通过上述两种方案最终得到的铜的质量:方案一_____(填“>”或“=”或“<”)方案二。以上两种方案中,方案二优越于方案一,理由是________(答一点)。
(拓展探究)在方案一中,小明和小丽分别取24克氧化铜,用CO还原,小明得到19.2克红色固体,小丽得到20.8克红色固体。为什么两人得到的红色固体质量不相等?
查阅资料:
Ⅰ.CO还原CuO时也可产生红色的氧化亚铜(Cu2O)
Ⅱ.Cu2O+H2SO4(稀)=Cu+CuSO4+H2O
他们分析推断:
④一致认为________(填“小明”或“小丽”)的产物中肯定含有Cu2O;
⑤用CO还原4克CuO得到红色固体a克,若红色固体为Cu和Cu2O的混合物,则a的取值范围为____________;
⑥可以用简单的实验验证红色固体中是否有Cu2O,请简述操作、现象及结论:_____。
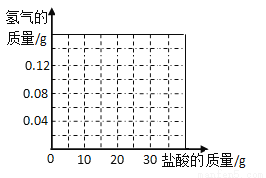
(6)我国约在南北朝时就开始冶炼黄铜。黄铜是铜和锌的合金(Cu-Zn),它可用来制造电器零件及日用品。为了测定某黄铜样品中铜的质量分数(不考虑黄铜中的其他杂质),现将30g稀盐酸分三次加入到10g黄铜样品粉末中,每次充分反应后,测定本次生成氢气的质量,实验数据见表。试求:
第一次 | 第二次 | 第三次 | |
加入稀盐酸的质量(g) | 10 | 10 | 10 |
本次生成氢气的质量(g) | 0.04 | m | 0.02 |
①m=____________。
②此黄铜样品中铜的质量分数是多少_______?。
③稀盐酸的溶质质量分数是_______。
④在坐标系中画出生成氢气总质量与加入盐酸质量关系的图像。______