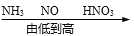下列实验操作中不能达到实验目的的是
选项 | 物质 | 主要实验操作 |
A | 鉴别NH4NO3固体和NaOH固体 | 分别加水溶解,测溶液的温度变化 |
B | 除去CO2中混有少量CO | 缓缓通过灼热的氧化铜 |
C | 检验CH4中是否含有H2 | 点燃,在火焰上方罩一干冷烧杯,观察烧杯壁上是否有水滴产生 |
D | 除去FeSO4溶液中的CuSO4 | 加入过量的铁粉,过滤 |
A. A B. B C. C D. D
化学与生活、生产密切相关。
(1)我国首架大型客机C919中使用了大量的铝镁合金,铝制品在空气中不易被腐蚀,具有“自我保护”能力,其原因是_____(用化学方程式表示)。
(2)铝、铜、银是日常生活中接触到的三种金属。同学甲设计了如下三个实验来验证它们的金属活动性强弱:① 铝、硝酸银溶液;②铜、硫酸铝溶液;③铜、硝酸银溶液。同学乙认为这一方案中实验 ______(填“①”、“②”、“③”)可以不做,也能验证三个金属的活动性强弱。请写出实验③中的实验现象______。
(3)中国南海海底有大量的可燃冰(CH4·nH2O)。
① 可燃冰中,水分子形成一种空间笼状结构,甲烷和少量N2、CO2等分子填入笼内空隙中,无固定的化学计量关系,因此可燃冰属于________(选填“纯净物”或“混合物”)。
②甲烷在一定量的氧气中燃烧,测得反应前后各物质的质量如下表所示:
物质 | 甲烷 | 氧气 | 水 | 二氧化碳 | 一氧化碳 |
反应前质量/g | 3.2 | 11.2 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 7.2 | 4.4 | 未测 |
根据表格中数据,请完成甲烷在一定量的氧气中燃烧的化学方程式 _______。
(4)某工厂利用废硫酸与废铁屑反应制取硫酸亚铁。现制得FeSO4 1.52 t,需要铁的质量至少是多少?(在答题卡上写出计算过程)_______
水是生命之源,人类的生产、生活都离不开水。
(1)自然界中的水含有许多可溶性和不溶性杂质。长期饮用硬水可能会引起体内结石,生活中常用____________的方法来降低水的硬度。
(2)水是常用的溶剂,配制下列溶液时,以水做溶剂的是_______(填序号)。
A.生理盐水 B.医用碘酒 C.高锰酸钾溶液 D.医用酒精
(3)下表是NaCl、KNO3在不同温度时的溶解度
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
①根据表中的数据,在坐标纸上绘制出氯化钠和硝酸钾两种物质的溶解度曲线。(请用铅笔在答题卡的坐标纸上绘图)________
②根据绘制的氯化钠和硝酸钾的溶解度曲线判断,温度大约在_____℃时,两种物质的溶解度大小相等。
③现有氯化钠和硝酸钾各40g ,30℃时,分别加入两只盛有100g水的烧杯中,能得到饱和溶液的是______(填溶质名称), 将上述得到的不饱和溶液转化为该温度下的饱和溶液,可采用的方法是_____。
④在60℃时,硝酸钾的溶解度是110g。这句话的含义是______。
(4)以太阳能为热源,经由铁氧化合物循环分解水的过程如右图所示:

① 写出在一定条件下发生的反应Ⅱ的化学方程式______。
② 在上述循环过程中,最终得到的产品是________。
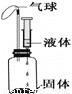
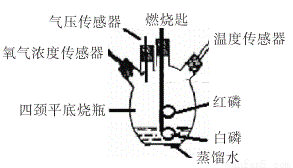
拉瓦锡曾经做了这样一个实验:让水蒸气通过一根烧红的枪管,生成了一种气体。同学们对这个实验很感兴趣,设计了如图所示的装置进行探究:在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”(石棉绒是耐高温材料,不与水和铁反应)。

(1)反应一段时间后,有肥皂泡吹起时,用点燃的火柴靠近肥皂泡,当听到有爆鸣声时,说明“铁与水蒸气”能够进行反应,生成_____(写化学式)。
(2)实验中石棉绒的作用是 _______ 。
(3)探究玻璃管中剩余固体成分是什么?
(查阅资料)1.常见铁的氧化物的性质
常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
能否被磁铁吸引 | 否 | 否 | 能 |
与稀硫酸反应 | 生成FeSO4 | 生成Fe2(SO4)3 | 生成FeSO4 、Fe2(SO4)3 |
2.铁可与硫酸铁溶液反应生成硫酸亚铁。
(初步验证)玻璃管中剩余固体为黑色,能全部被磁铁吸引。
(猜想与假设)猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是_______。
(实验探究)
实验操作 | 实验现象 | 实验结论 |
将玻璃管中的剩余固体取出,放入试管中,加入过量的稀硫酸。 | 有气泡产生 | ______ |
(反思与交流)往剩余固体中加入过量的稀硫酸后,若无气体产生,你_______(填“能”或“不能”)确定剩余固体成分,原因是________。
 B. 物质的溶解性:
B. 物质的溶解性:
 D. 氮元素化合价:
D. 氮元素化合价: