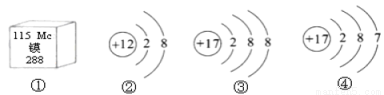
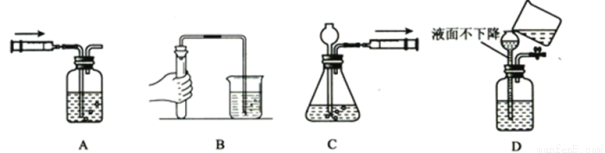
下列归纳和总结完全正确的一组是
A.对物质鉴别的认识 | B.对物质性质与用途的认识 |
①用肥皂水鉴别硬水和软水 ②用带火星的木条鉴别空气和呼出气体 | ①氧气能支持燃烧,可用作燃料 ②氮气化学性质稳定,可做保护气 |
C.对现象的认识 | D.对概念的认识 |
①气体可压缩贮存于钢瓶中,证明分子之间有间隔 ②水受热蒸发变成水蒸气,水分子的化学性质保持不变 | ①质子数相同的粒子,一定属于同种元素 ②同种元素组成的物质,一定是单质 |
A. A B. B C. C D. D
一定条件下,密闭容器内发生的某化学反应,测得t1和t2时各物质的质量见表,下列说法正确的是
物质 | M | N | P | Q |
t1时的质量/g | 51 | 9 | 3 | 17 |
t2时的质量/g | 23 | 3 | x | 51 |
A. P一定是催化剂 B. Q可能是单质
C. 该反应一定是分解反应 D. M与N的质量变化比为14:3
化学就在我们身边,它与我们的生活息息相关。
(1)按要求用化学式填空:
①空气中含量最多的物质_________;②地壳中含量最多的非金属元素和金属元素组成的物质的化学式_________;③能使澄清石灰水变浑浊的气体____________;④相对分子质量最小的氧化物____________
(2)天然水中含有的部分杂质如下表所示,请根据表中内容回答问题。
溶解物质 | 悬浮物质 | |
主要气体 | 主要离子 | 细菌、藻类、 泥沙、黏土 |
氧气、二氧化碳、硫化氢 | 钙离子、氯离子、硫酸根离子、钠离子 |
①上表中“主要气体”中属于氧化物的气体有___________种;
②写出“主要离子”中一种阴离子的符号____________;
③水的硬度是一项重要的化学指标,生活中常用__________的方法来降低水的硬度;
④若要除去该水样中的颜色和臭味,可加入物质是____________。
合成氨是人类科学技术上的一项重大突破,对社会发展与科技进步做出了巨大贡献。合成氨工艺的主要流程如下:
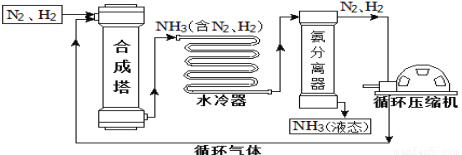
(1)合成塔中的反应必须在高温、高压、催化剂条件下进行,该反应的化学方程式是:________
(2)生产过程中可重复使用的物质是_______________(填化学式)。
(3)根据表中的数据回答问题。
物质 | H2 | N2 | O2 | NH3 |
沸点/℃(1.01×105 Pa) | –252 | –195.8 | –183 | –33.35 |
在1.01×105 Pa时,要将产物NH3与N2、H2分离开来,最适宜的温度应该控制在_________℃。
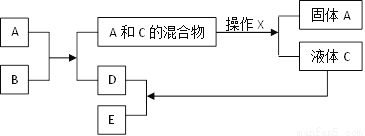
(4)下图是合成塔中发生反应的微观粒子示意图:
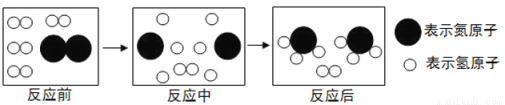
由图可知两种反应物N2与H2的分子个数比为____________;该反应中的最小粒子是_________(填写化学符号)。
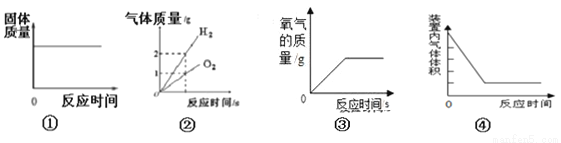
“化学反应条件的控制是实验灵魂”。小林和同学在老师指导下,探究了“影响过氧化氢分解速度的因素”。
(实验)
(1)取两支大试管,分别倒入适量的5%、10%的过氧化氢溶液,再加入等量的二氧化锰,各收集一集气瓶气体,发现浓度大的先收集满。该操作过程中合理的排列顺序____________。(选填序号)
①检验装置的气密性 ②旋紧连有导管的单孔塞
③将水槽中待收集气体的集气瓶注满水 ④有连续稳定气泡再排水集气
⑤向大试管内倒入适量过氧化氢溶液再加入少许二氧化锰粉末
(2)取a 、b两支试管加入等体积5%的过氧化氢溶液,再分别加入少许二氧化锰粉末、氧化铜(CuO)粉末,发现a 中比b中产生气泡多且快。随即用带火星的木条分别悬空伸入试管内,发现a中火星复燃,b中火星仅发亮但不复燃。
( 结论)
根据实验(1)(2)得出影响过氧化氢溶液分解的因素是________________、_____________。
(反思) “红砖粉末是否也可以作过氧化氢分解的催化剂?”
(实验)实验步骤和现象如下:
①小林分别向两支试管中加入等质量等浓度的过氧化氢溶液,向其中一支试管加入一药匙红砖粉末,然后将两支试管中的气体通入水中比较产生气泡的快慢,发现加入红砖粉末的试管中反应较快。
②将反应较快的试管内固体过滤出来,洗涤、烘干。
③用烘干后的固体重复步骤①的实验,现象与步骤①完全相同。
试回答:步骤③的实验目的是___________________________。小林认为通过上述实验已证明红砖粉末可以作过氧化氢分解反应的催化剂,但老师认为小林同学的实验还缺少一个关键步骤,请指出来_______________________________________。
(拓展提高)
小林在实验时,联想到了卖鱼卖虾的商贩用过氧化钙(CaO2)增加水池中的含氧量,于是提出如下猜想.
(猜想)过氧化钙与水反应可制取氧气.
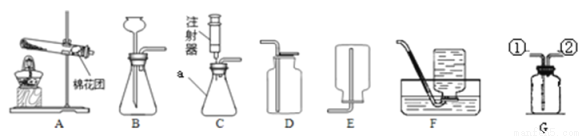
实验装置 | 实验主要过程 |
| ①检查装置气密性. ②加入过氧化钙和水后,有少量细小气泡缓慢放出,在导管口几乎收集不到气体.该装置放置到第二天,集气瓶中只收集到极少量气体,震荡试管后仍有少量细小气泡缓慢放出. |
实验结论:过氧化钙与水反应____________(填“能”或“不能”)用于实验室制取氧气.
(分析与反思)
(1)过氧化钙与水反应虽然没有快速收集到大量氧气,但由此实验现象,小林认为商贩用过氧化钙做增氧剂的主要原因是______________________.
(2)小林希望对此实验进行改进,使该反应加快,请你帮他提出合理化建议_____________.
(计算)该兴趣小组的同学们购得用于增氧的过氧化钙产品(杂质不含钙元素),标签如图所示.试计算:

(1)过氧化钙的相对分子质量为_____________;
(2)过氧化钙中钙元素与氧元素的质量比为____________;
(3)过氧化钙与水反应生成氢氧化钙和氧气,______g过氧化钙与37g氢氧化钙含钙量相当;
(4)该产品(如图)中过氧化钙的质量分数至少为_____________.