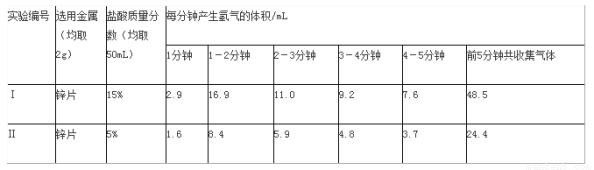
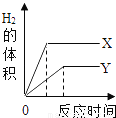
某食品包装袋中有一个小纸袋,上面写“生石灰干燥剂,请勿食用”。该食品已放置两月有余。请你对下列问题进行探究。
(1)小纸袋中的物质能否继续作干燥剂?
实验步骤 | 实验现象 | 结论 |
取足量的小纸袋中的固体放入烧杯中,加入适量的水,触摸杯壁 |
| 可继续作干燥剂 |
(2)猜想:小纸袋中的物质除含有CaO外,还可能含有Ca(OH)2和 ;
(3)请设计实验证明(2)中你所填的物质是否存在。
(1)固体慢慢变为糊状物质,且放出大量的热(2)碳酸钙(3)取少量纸袋内的固体放在试管中,加入适量盐酸,如果能够产生大量的气泡说明其中含有碳酸钙。 【解析】 试题可继续作干燥剂说明其中的氧化钙没有变质,因此氧化钙加入水后会发生和水的反应,反应中放出大量的热,因为氧化钙很容易吸收水分发生和水的反应,因此固体中可能含有氢氧化钙,而氢氧化钙很容易与空气中的二氧化碳反应产生碳酸钙沉淀,所以固体...