氯化铵(NH4Cl)是一种重要的化工原料。
(1)氯化铵可用作_________肥。
(2)氯化铵的溶解度如表所示:
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
溶解度/g | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | 77.3 |
60℃时,向盛有45.8g NH4Cl的烧杯中,加入100g的水,充分路解后形成溶液的是_________(填“饱和”或“不饱和“),若要达到饱和,可采用的方法是①加NH4Cl_________g,或②_________℃
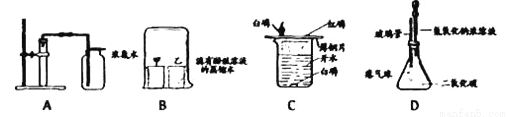
(3)如图所示,小烧杯中盛放的是②中所得的饱和溶液。若将少量的下列物质分别小心地加入到大烧杯的水中,不断搅拌,能够使小烧杯中有固体析出的是_________(填字母)。
A.冰 B.氢氧化钠 C.硝酸铵 D.氧化钙

将一段去除氧化镁的镁条放入一定量的盐酸中,有气泡产生,充分反应后静置,发现试管中有白色沉淀产生。为探究白色沉淀的成分,9 (1)班兴趣小组同学在老师的指导下进行如下实验:
试管(盛有等体积等浓度的盐酸) | ① | ② | ③ | ④ |
镁条质量(g) | 1 | 1.5 | 2 | 2.5 |
实验现象 | 快速反应,试管发热,镁条全部消失 | |||
白色沉淀量(恢复至20℃) | 无 | 少量 | 较多 | 很多 |
(1)4支试管中盛有等体积等浓度的盐酸的原因________________。
(得出结论)(2)镁条与盐酸反应产生白色沉淀的量与________________有关。
(提出问题)白色沉淀是什么物质?
(查阅资料)在氯化镁溶液中,镁能与水常温下反应生成氢氧化镁和氢气。
(猜想与假设)
甲:白色沉淀可能是碳酸镁
乙:白色沉淀可能是生成的氯化镁增多析出的晶体
丙:白色沉淀可能是剩余的镁
丁:白色沉淀可能是氢氧化镁
(3)其他同学认为甲的猜想是错误的,原因是________________
(实验验证)
序号 | 操作步骤 | 实验现象 | 结论 |
1 | 取第一份白色不溶物于试管中,加入蒸馏水,震荡 | (4)沉淀________________溶解(选填会或不会) | 乙同学猜想不成立 |
2 | 取第二份白色不溶物于试管中,加入稀盐酸 | (5)________________ | 丙同学猜想不成立 |
3 | ①取第三份白色不溶物于试管中,加入稀硝酸 ②向所得溶液加入几滴硝酸银溶液 | ①白色沉淀不溶解 ②出现大量白色沉淀 | ①丁同学猜想不成立 ②白色不溶物一定含(6)________________元素 |
(7)在老师的帮助下,同学们得出白色沉淀物是Mg2(OH)2Cl2反应的化学方程式为2Mg+2HCl+2H2O=Mg2(OH)2Cl2+2X则X为________________。
(拓展延伸)
小钢同学认为上述实验验证3的设计不严密,在实验验证3之前应该对不溶物进行洗涤,目的是________________。
便于对比。镁条质量。反应物中不含有碳元素,不可能生成碳酸镁。不会不产生气泡白色不溶物一定含氯元素H2。排除氯离子的干扰。 【解析】 (1)用控制变量法做探究实验时,要保证其他因素相同,只留一个变量,这样才便于对比,得出准确的结论。(2)由表格数据可知,在盐酸的体积和浓度相同的条件下,镁条质量越大,产生白色沉淀的量越多。(3)根据质量守恒定律可知,反应前没有碳元素,反应后就得不到碳酸镁。...化学兴趣小组的同学发现实验台上一瓶标签破损的无色溶液(标签如图)。

(猜想与假设)
小宁:可能是氢氧化钠溶液
小静:可能是(1)__________溶液
小致:可能是(2)__________溶液
小远同学认为小宁的猜想不可能,原因是(3)__________。
(实验探究)
实验操作 | 实验现象 | 结论 |
取该溶液少许,滴加(4)__________ | 有气泡产生 | (5)__________同学的猜想成立。 |
(反思与评价)
标签为什么会破损,小静同学想测定该溶液的酸碱度,她的操作步骤是:(6)__________。测得溶液的pH,(7)__________(选填>7,=7或<7),溶液显__________性(选填酸性、中性或碱性)致使标签破损。
Na2CO3;Na2SO4;因为氢氧化钠化学式中Na右下方没有2;稀盐酸;小静;在玻璃片上放一片pH试纸,用玻璃棒蘸取待测液滴到pH试纸上,立即与标准纸比色卡比较,读出溶液的pH值>7;碱性; 【解析】 (1)(2)由破损的标签图可知,该无色溶液的阳离子为钠离子,且阴离子的化合价为-2价,则该无色溶液可能是Na2CO3或Na2SO4;(3)氢氧化钠的化学式为NaOH,Na的右下角没有“...