请从A、B两题中任选一个作答。若两题均答,按A计分。
题号 | A | B |
实验目的 | 探究_________ | 探究________ |
实验装置 |
|
|
实验原理 | (1)化学方程式是_______ | (1)化学方程式是_______ |
部分实验现象 | (2)溶液蓝色逐渐变浅,天平指针_______; | (2)如图,缓慢打开左端活塞,a处可观察到_______; |
小明通过实验证明二氧化碳能与氢氧化钠反应,并检验生成了碳酸盐。
25℃时,氢氧化钠和碳酸钠在乙醇中的溶解度如下表所示。
物质 | NaOH | Na2CO3 |
溶解度/g | 17.3 | <0.01 |
利用如图所示装置进行实验(该装置气密性良好;乙醇不参与反应)。

[步骤1]打开K1,关闭K2,从a口通入二氧化碳,看到饱和氢氧化钠的乙醇溶液中产生大量沉淀,停止通二氧化碳;
[步骤2]从a口通入氮气,直至排净装置中的二氧化碳;
[步骤3]关闭K1,打开K2,向甲装置的试管中滴入足量的稀盐酸。
(1)步骤1装置甲的试管中能看到沉淀的原因是______。
(2)步骤2中,排净装置甲中二氧化碳的目的是______。
(3)步骤3乙中能看到的现象是________,反应的化学方程式是_______。
二氧化碳与氢氧化钠反应生成碳酸钠,碳酸钠在乙醇中的溶解度比氢氧化钠小很多 避免装置内残留的二氧化碳对后面实验的干扰 石灰水变浑浊 CO2 + Ca(OH)2 = CaCO3↓ + H2O 【解析】(1)二氧化碳与氢氧化钠反应生成碳酸钠,碳酸钠在乙醇中的溶解度比氢氧化钠在乙醇中的溶解度小很多,不能溶解的碳酸钠析出,所以会看到沉淀。(2)步骤2中,排净装置甲中二氧化碳的目的是避免装置内残留的二氧...



 4NO₂↑+O₂↑+_____。
4NO₂↑+O₂↑+_____。
 4NO₂↑+CO₂↑+2H2O。
4NO₂↑+CO₂↑+2H2O。 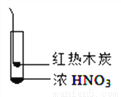
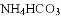 B.
B. 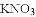 C.
C.  D.
D. 