0 172543 172551 172557 172561 172567 172569 172573 172579 172581 172587 172593 172597 172599 172603 172609 172611 172617 172621 172623 172627 172629 172633 172635 172637 172638 172639 172641 172642 172643 172645 172647 172651 172653 172657 172659 172663 172669 172671 172677 172681 172683 172687 172693 172699 172701 172707 172711 172713 172719 172723 172729 172737 211419
 高温煅烧一定质量的石灰石
高温煅烧一定质量的石灰石 用等质量、等浓度的双氧水分别制取氧气
用等质量、等浓度的双氧水分别制取氧气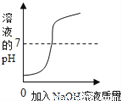 向一定体积的水中逐滴加入氢氧化钠溶液
向一定体积的水中逐滴加入氢氧化钠溶液 某温度下,向一定量不饱和硝酸钾溶液中加入硝酸钾晶体
某温度下,向一定量不饱和硝酸钾溶液中加入硝酸钾晶体



