化学课后,化学兴趣小组的同学在整理实验桌时,发现有一瓶氢氧化钠溶液没有塞橡皮塞,征得老师同意后,开展了以下探究:
[提出问题1] 该氢氧化钠溶液是否变质了呢?
[实验探究1]
实验操作 | 实验现象 | 实验结论 |
取少量该溶液于试管中,向溶液中滴加稀盐酸,并不断振荡。 | _____________ | 氢氧化钠溶液一定变质了。 |
[提出问题2] 该氢氧化钠溶液是全部变质还是部分变质呢?
[猜想与假设]
猜想1:氢氧化钠溶液部分变质。 猜想2:氢氧化钠溶液全部变质。
[查阅资料] ⑴ 氯化钙溶液呈中性。
⑵ 氯化钙溶液能与碳酸钠溶液反应(方程式):________________________。
[实验探究2]
实验步骤 | 实验现象 | 实验结论 |
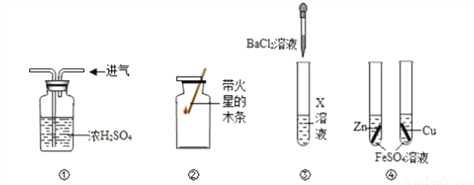
⑴取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,并不断振荡。 | 有________生成 | 说明原溶液中一定有碳酸钠。 |
⑵取步骤⑴试管中的少量上层清液,滴加酚酞溶液。 | _____________ | 说明原溶液中一定有______。 |
[实验结论] 该氢氧化钠溶液_______(填“部分”或“全部”)变质。
[反思与评价] ⑴氢氧化钠溶液露置于空气中容易变质,请写出相关反应的化学方程式:_________。
⑵在上述[实验探究2]中,小明提出可用氢氧化钙溶液代替氯化钙溶液,你认为该方案________(填“可行”或“不可行”)。
[理解与应用] 氢氧化钠溶液容易变质,必须密封保存。
有气泡冒出 Na2CO3+CaCl2= CaCO3+ 2NaCl 白色沉淀生成; 变红 氢氧化钠; 部分变质 2NaOH+CO2===Na2CO3+H2O 不可行 【解析】氢氧化钠变质后生成碳酸钠,故加入稀盐酸后,一定有气泡冒出; 氯化钙与碳酸钠反应生成碳酸钙和氯化钠,反应方程式为Na2CO3+CaCl2= CaCO3+ 2NaCl 原溶液中有碳酸钠,则加入氯化钙后有白色沉淀生成... ______________________
______________________ _____________________
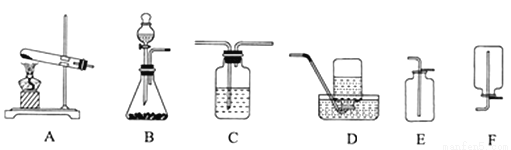
_____________________
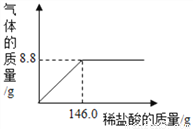
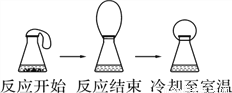
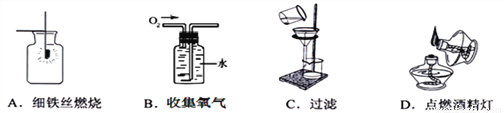
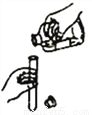 倾倒液体 B.
倾倒液体 B. 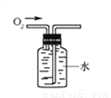 收集氧气
收集氧气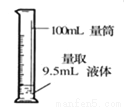 量取液体 D.
量取液体 D. 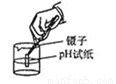 测量 pH
测量 pH