四氧化三铁可用于医疗器械、电子等工业。某实验兴趣小组从工厂采集废液(含FeSO4和少量ZnSO4、MgSO4),进行四氧化三铁的制备实验。
【阅读资料】
(1)25℃时,去氧化物沉淀的pH范围如表。
Zn(OH)2 | Fe(OH)2 | Mg(OH)2 | |
开始沉淀的pH | 5.7 | 7.6 | 10.4 |
沉淀完全的pH | 8.0 | 9.6 | 12.4 |
(2)25℃时,Zn(OH)2可溶于pH>10.5的碱溶液。
(3)制备Fe3O4的实验流程如下:
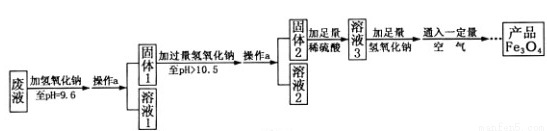
【回答问题】
(1)往废液中加入氢氧化钠溶液生成沉淀的化学方程式为 (写一个即可)。
(2)操作a的名称为 。该操作需要的玻璃仪器有烧杯、玻璃棒、 等。玻璃棒在此操作中的主要作用是 。
(3)溶液1所含溶质有 (至少写两种);溶液3所含溶质的主要成分为 。
(4)该实验取废液100g,最终得到产品四氧化三铁质量为3.48g,则原废液中硫酸亚铁溶质的质量分数不低于 (精确到0.01%)。
⑴2 NaOH+ ZnSO4= Zn(OH)2↓ +Na2SO4或2 NaOH+ FeSO4= Fe(OH)2↓ +Na2SO4⑵过滤、漏斗、引流(搅拌)⑶硫酸镁、硫酸钠、氢氧化钠、氢氧化镁(两种即可)、硫酸亚铁 ⑷6.84% 【解析】(1)第一步加氢氧化钠至PH=9.6,结合阅读资料可知会生成两种沉淀。它们分别是Zn(OH)2和Fe(OH)2,并且二者全部沉淀。可写2 NaOH+ ZnSO...在青海的茶卡盐湖,沿湖居民“夏天晒盐、冬天捞碱”,“盐”指的是食盐,“碱”指的是纯碱。
以下是碳酸钠、氯化钠在不同温度下的溶解度
0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 80℃ | 100℃ | |
S(Na2CO3)/g | 7.0 | 12.2 | 21.8 | 39.7 | 48.8 | 47.3 | 46.4 | 45.1 | 44.7 |
S(NaCl)/g | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 38.4 | 39.8 |
(1)“冬天捞碱”的原理是_______________________________。
(2)盐湖中获取的纯碱(天然碱)中一般含有一定量的氯化钠,现有标注为“纯度80%”的天然碱,要提纯碳酸钠,操作步骤如下:
①在50g40℃的热水中加入一定质量的天然碱,配成40℃时碳酸钠的饱和溶液;
(不考虑不同溶质之间的相互影响)
②降温至10℃,析出一定质量的碳酸钠晶体,过滤,用少量水洗涤晶体;
③将碳酸钠晶体烘干后,获得__________g碳酸钠粉末。(不考虑洗涤过程中碳酸钠的损耗)
(3)某学习小组同学要测定天然碱中碳酸钠的质量分数是否与标注符合,进行如下实验:
①称取5g天然碱放入锥形瓶内,再向其中加入50g溶质质量分数为10%的稀盐酸,充分反应后,称得烧杯内物质总质量为53.5g,请根据实验计算出天然碱中碳酸钠的质量分数为______。(结果保留到0.1%)
②思考:实验结果小于标注的原因可能是_______________________________________。
(4)上述实验中所需的50g溶质质量分数为10%的稀盐酸,需要用市售的37%的浓盐酸进行配制。请计算出配制时需要浓盐酸___________g、水___________g。(结果保留至0.1)
温度低于40℃时,温度降低,碳酸钠的溶解度减小,析出晶体 18.3 72.0%(或72.3%) 有部分二氧化碳溶于水或没有逸出锥形瓶,导致结果偏小 13.5 36.5 【解析】本题考查了根据化学反应方程式的计算;结晶的原理、方法及其应用;有关溶质质量分数的简单计算。 (1)“冬天捞碱”的原理是:温度低于40℃时,温度降低,碳酸钠的溶解度减小,析出晶体; (2)由物质的溶解度可知,...同学们在学习碱的化学性质时,进行了如下图所示的实验。

(1)甲实验中,在用稀盐酸和氢氧化钠溶液进行中和反应实验时,溶液的酸碱度变化如下图所示。

①该实验操作是将 ___________溶液滴加到另一种溶液中。
②当加入溶液的质量为ag时,所得溶液中的溶质为(写化学式)_________。
③当加入溶液的质量为bg时,向所得溶液中滴加酚酞溶液,溶液呈_______色。
(2)乙实验中滴加氢氧化钠溶液后,可观察到的现象是_______________________________________。
(3)丙实验中观察到试管内有白色沉淀产生。
(4)实验结束后,同学们将甲、乙、丙三个实验的废液倒入同一个干净的废液缸中,最终看到废液浑浊并呈红色,产生疑问。
【提出问题】 废液中含有哪些物质?
【交流讨论】
①一定含有的物质:碳酸钙、指示剂、水和_______________。
②还含有能使废液呈碱性的物质。能使废液呈碱性的物质是什么?同学们有如下猜想。
小云认为:只有碳酸钠
小红认为:只有氢氧化钙
小林认为:是氢氧化钠和碳酸钠
你认为还可能是______________ 。(写一种猜想)
【实验设计】
小方想利用氯化钙溶液来验证小云、小红、小林的猜想。查阅资料获悉氯化钙溶液呈中性,并设计如下实验。请你将小方的实验设计补充完整。________________
实验内容 | 预计现象 | 预计结论 |
取少量废液缸中上层清液于试管中,加入过量氯化钙溶液,静置。 | ①__________。 | 小云的猜想正确。 |
②___________。 | 小红的猜想正确。 | |
③___________。 | 小林的猜想正确。 |

