19.某化学兴趣小组取用生石灰时,发现装生石灰(CaO)的塑料试剂瓶已经膨胀破裂.他们请教老师后得知该生石灰已经变质.他们对瓶内固体的成分产生了好奇,于是他们对这瓶固体的成分展开了探究.
【提出问题】这瓶久置的生石灰的成分是什么?
【猜想假设】猜想一:全部是Ca(OH)2
猜想二:是CaO和Ca(OH)2的混合物
猜想三:是Ca(OH)2和CaCO3的混合物
你还可以作出的猜想是:CaO、Ca(OH)2和CaCO3的混合物或CaCO3
【查阅资料】Ca(OH)2微溶于水,能与稀盐酸反应生成氯化钙和水.
【分析判断】该固体可能含有Ca(OH)2的原因是CaO+H2O═Ca(OH)2(用化学方程式表示)
【实验探究】
写出操作②中发生的化学反应方程式CO2+Ca(OH)2═CaCO3↓+H2O.
【实验结论】
通过以上实验探究,得出猜想三成立.
【拓展迁移】
小组同学反思了生石灰干燥剂变质的原因,认识到实验室保存氧化钙应注意密封保存.
【数据处理】
为测定该固体中碳酸钙的质量分数,取样品10g于烧杯中加入稀盐酸50g,恰好完全反应,反应后烧杯中物质总质量为56.7g,则该固体中碳酸钙的质量分数是75%(写出具体的计算过程).
【提出问题】这瓶久置的生石灰的成分是什么?
【猜想假设】猜想一:全部是Ca(OH)2
猜想二:是CaO和Ca(OH)2的混合物
猜想三:是Ca(OH)2和CaCO3的混合物
你还可以作出的猜想是:CaO、Ca(OH)2和CaCO3的混合物或CaCO3
【查阅资料】Ca(OH)2微溶于水,能与稀盐酸反应生成氯化钙和水.
【分析判断】该固体可能含有Ca(OH)2的原因是CaO+H2O═Ca(OH)2(用化学方程式表示)
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量固体,倒入适量水,充分搅拌、静置 | 无放热现象 | 固体中一定不含CaO |
| ②取上层清液于试管中,通入二氧化碳 | 变浑浊 | 固体中一定含Ca(OH)2 |
| ③另取少量固体放入试管中,加入稀盐酸 | 有气泡冒出 | 固体中一定含CaCO3 |
【实验结论】
通过以上实验探究,得出猜想三成立.
【拓展迁移】
小组同学反思了生石灰干燥剂变质的原因,认识到实验室保存氧化钙应注意密封保存.
【数据处理】
为测定该固体中碳酸钙的质量分数,取样品10g于烧杯中加入稀盐酸50g,恰好完全反应,反应后烧杯中物质总质量为56.7g,则该固体中碳酸钙的质量分数是75%(写出具体的计算过程).
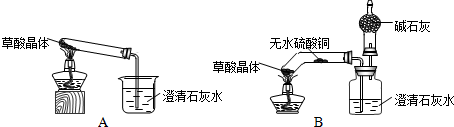
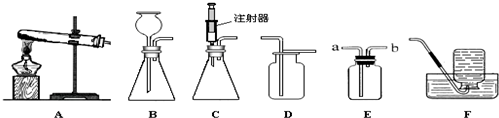
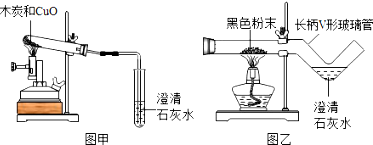
16.我国劳动人民早在五千年前就会使用木炭炼铜.在化学实验室里模拟炼铜,既可用传统的实验装置(见图甲),又能用改进的微型实验装置(见图乙).化学兴趣小组采用图乙装置,开展以下探究活动.
【提出问题】木炭与CuO反应所得红色固体中含有什么物质?
【查阅资料】
(1)写出木炭与CuO反应的化学方程式:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑,若该反应进行的不彻底,产物中还有氧化亚铜(Cu2O,红色固体).
(2)Cu不溶于稀硫酸,Cu2O能与稀硫酸反应得到蓝色CuSO4溶液:Cu2O+H2SO4═Cu+CuSO4+H2O.
【作出猜想】红色固体的成分:①全部是Cu;②全部是Cu2O;③既有Cu也有Cu2O.
【实验探究】
(1)取木炭、CuO两种黑色粉末适量,再加少许CaC12(能降低反应温度,加快反应速率)均匀混合,然后将黑色粉末装入长柄V形玻璃管的直管内.
(2)按图乙连好实验装置,然后加热反应物;2分钟后,黑色粉末出现红热现象,同时澄清的石灰水变浑浊,此时停止加热.
(3)待玻璃管冷却后,提取里面的红色固体,进行如下的验证:(相对原子质量Cu-64 O-16)
【评价反思】
(1)使用图乙装置与使用图甲装置相比,其优点是节约药品(写出1条即可).
(2)若要证明CaC12是该反应的催化剂,还需要验证CaCl2的质量和化学性质在反应前后不变.

【提出问题】木炭与CuO反应所得红色固体中含有什么物质?
【查阅资料】
(1)写出木炭与CuO反应的化学方程式:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑,若该反应进行的不彻底,产物中还有氧化亚铜(Cu2O,红色固体).
(2)Cu不溶于稀硫酸,Cu2O能与稀硫酸反应得到蓝色CuSO4溶液:Cu2O+H2SO4═Cu+CuSO4+H2O.
【作出猜想】红色固体的成分:①全部是Cu;②全部是Cu2O;③既有Cu也有Cu2O.
【实验探究】
(1)取木炭、CuO两种黑色粉末适量,再加少许CaC12(能降低反应温度,加快反应速率)均匀混合,然后将黑色粉末装入长柄V形玻璃管的直管内.
(2)按图乙连好实验装置,然后加热反应物;2分钟后,黑色粉末出现红热现象,同时澄清的石灰水变浑浊,此时停止加热.
(3)待玻璃管冷却后,提取里面的红色固体,进行如下的验证:(相对原子质量Cu-64 O-16)
| 步骤 | 现象 | 结论 |
| ①取1.44g红色固体装入试管,滴入足量的稀硫酸,充分反应 | 红色固体部分减少,溶液变 为蓝色 | 猜想①错误 |
| ②滤出试管中残留的红色固体,洗涤干燥,称其质量为1.04g | 猜想③正确 |
(1)使用图乙装置与使用图甲装置相比,其优点是节约药品(写出1条即可).
(2)若要证明CaC12是该反应的催化剂,还需要验证CaCl2的质量和化学性质在反应前后不变.
14.下列化学方程式书写正确的是( )
| A. | 镁条燃烧:Mg+O2$\frac{\underline{\;点燃\;}}{\;}$MgO2 | |
| B. | 实验室制氧气:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2 | |
| C. | 硫酸铜和氢氧化钠反应:CuSO4+2NaOH═Cu(OH)2+Na2SO4 | |
| D. | 天然气燃烧:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O |
13.某研究性学习小组的同学前往当地的石灰石矿区进行调查,他们取了若干块矿石样品,对样品中的碳酸钙的质量分数进行检测,采用了以下的办法:取用8g这种石灰石样品,把40g稀盐酸分四次加入,测量过程所得数据见下表(杂质不溶于水,不与盐酸反应).
请计算:
(1)哪几次反应中碳酸钙有剩余一、二;
(2)上表中的m的数值应为1.2;
(3)这种石灰石中碳酸钙的质量分数为多少?(写出计算过程)
0 169205 169213 169219 169223 169229 169231 169235 169241 169243 169249 169255 169259 169261 169265 169271 169273 169279 169283 169285 169289 169291 169295 169297 169299 169300 169301 169303 169304 169305 169307 169309 169313 169315 169319 169321 169325 169331 169333 169339 169343 169345 169349 169355 169361 169363 169369 169373 169375 169381 169385 169391 169399 211419
请计算:
| 加入稀盐酸的次序 | 第一次 | 第二次 | 第三次 | 第四次 |
| 加入稀盐酸的质量/g | 10 | 10 | 10 | 10 |
| 剩余固体的质量/g | 5.5 | 3.0 | 1.2 | m |
(2)上表中的m的数值应为1.2;
(3)这种石灰石中碳酸钙的质量分数为多少?(写出计算过程)