16. 铜器是生活中常见物品,铜器保存不善,表面会生成一层绿色铜锈.某化学兴趣小组同学欲通过实验来探究它的性质和组成.已知:
铜器是生活中常见物品,铜器保存不善,表面会生成一层绿色铜锈.某化学兴趣小组同学欲通过实验来探究它的性质和组成.已知:
Ⅰ.铜绿的主要成分是碱式碳酸铜:Cu2(OH)2CO3.
Ⅱ.铜器因所处环境不同,生成的铜绿中可能还含有CuSO4和CuC12.
Ⅲ.硫酸铜、氯化铜的化学性质稳定,酒精灯加热条件下不分解.
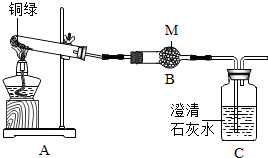
为了探究碱式碳酸铜的化学性质,该小组同学取少量铜绿(假设杂质不参与反应)按如图装置进行实验:
(1)M药品的名称是无水硫酸铜.
(2)实验过程中,发现A中绿色固体逐渐变为黑色,B中固体变蓝色,C中溶液变浑浊.写出Cu2(OH)2CO3分解的化学方程式Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+H2O+CO2↑.
(3)为了验证铜绿中是否有CuSO4和CuC12,该小组同学进行了如下实验,请补充完成下列实验报告:
 铜器是生活中常见物品,铜器保存不善,表面会生成一层绿色铜锈.某化学兴趣小组同学欲通过实验来探究它的性质和组成.已知:
铜器是生活中常见物品,铜器保存不善,表面会生成一层绿色铜锈.某化学兴趣小组同学欲通过实验来探究它的性质和组成.已知:Ⅰ.铜绿的主要成分是碱式碳酸铜:Cu2(OH)2CO3.
Ⅱ.铜器因所处环境不同,生成的铜绿中可能还含有CuSO4和CuC12.
Ⅲ.硫酸铜、氯化铜的化学性质稳定,酒精灯加热条件下不分解.
为了探究碱式碳酸铜的化学性质,该小组同学取少量铜绿(假设杂质不参与反应)按如图装置进行实验:
(1)M药品的名称是无水硫酸铜.
(2)实验过程中,发现A中绿色固体逐渐变为黑色,B中固体变蓝色,C中溶液变浑浊.写出Cu2(OH)2CO3分解的化学方程式Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+H2O+CO2↑.
(3)为了验证铜绿中是否有CuSO4和CuC12,该小组同学进行了如下实验,请补充完成下列实验报告:
| 步骤 | 操作 | 现象及结论 |
| ① | 取少量铜绿溶于足量稀硝酸中,并将溶液分成甲、乙两份 | 产生气泡 |
| ② | 向甲中滴加硝酸钡溶液 | 若观察到 产生白色沉淀,则铜绿中含有CuSO4 |
| ③ | 向乙中加入过量的硝酸钡溶液,振荡、静置,取上层清液于试管中,再滴加硝酸银溶液 | 若观察到产生白色沉淀,则铜绿中含有CuCl2 |
8.下列有关元素化合物的说法正确的是( )
| A. | 氧气是活泼的气体,能和所有物质发生氧化反应 | |
| B. | 若某气体在氧气中燃烧生成二氧化破和水,该气体一定是甲烷 | |
| C. | 硫酸能作干燥剂,可以干燥所有气体 | |
| D. | 盐酸、硫酸、醋酸有通性,因为它们在水中能电离出H+ |
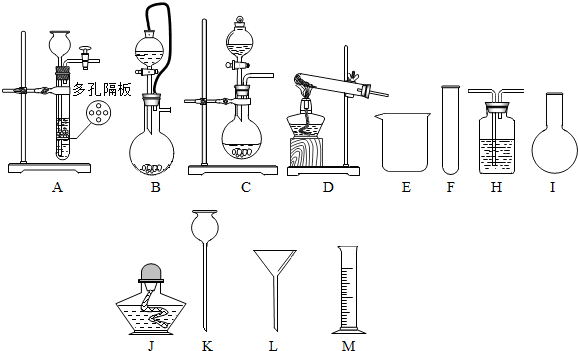
7.下列有关实验操作分析正确的是( )
0 168275 168283 168289 168293 168299 168301 168305 168311 168313 168319 168325 168329 168331 168335 168341 168343 168349 168353 168355 168359 168361 168365 168367 168369 168370 168371 168373 168374 168375 168377 168379 168383 168385 168389 168391 168395 168401 168403 168409 168413 168415 168419 168425 168431 168433 168439 168443 168445 168451 168455 168461 168469 211419
| 选项 | 实验操作 | 评价 |
| A | 稀释浓硫酸时,将浓硫酸注入水中,并用玻璃棒不断搅拌 | 正确;浓硫酸溶于水放出大量热量并且浓硫酸的密度大于水 |
| B | 为了节省氢气,制备氢气直接点燃 | 不正确;不纯氢气不能燃烧 |
| C | 公用胶头滴管使用前要先用蒸馏水洗涤 | 正确;避免取第二种试剂时发生安全事故 |
| D | 用醋酸溶液检验小苏打、苏打粉末 | 不正确;它们与醋酸溶液都不反应 |
| A. | A | B. | B | C. | C | D. | D |
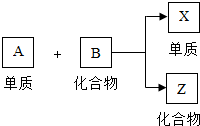 现有4种初中化学常见的物质,它们之间的转化关系如图所示(反应条件省略):
现有4种初中化学常见的物质,它们之间的转化关系如图所示(反应条件省略):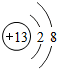 .则x的名称是铁.
.则x的名称是铁.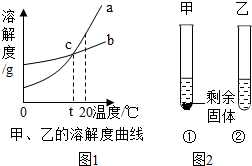 图1是甲、乙两种物质的溶解度曲线.20℃时,向两支试管中加入等质量的甲、乙两种固体物质,分别加入10g水,使其充分溶解,观察到如图2所示的现象.
图1是甲、乙两种物质的溶解度曲线.20℃时,向两支试管中加入等质量的甲、乙两种固体物质,分别加入10g水,使其充分溶解,观察到如图2所示的现象.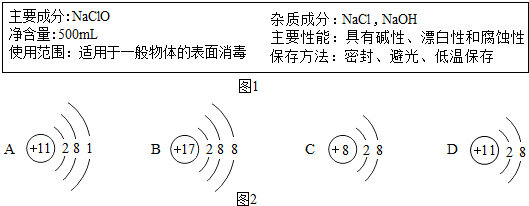
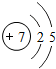 .
.