20.下列现象可用质量守恒定律解释的是( )
| A. | 10g水受热变成10g水蒸气 | |
| B. | 高锰酸钾受热分解后,固体的质量变小 | |
| C. | 水结冰后,体积增加 | |
| D. | 蜡烛受热熔化,冷却后质量不变 |
19.为了测定某赤铁矿样品(假设其中杂质不溶于水,也不与其他物质反应)中氧化铁的质量分数,小丽同学取一定质量的该矿石样品放入烧杯中,再取180g稀硫酸分三次加入烧杯中,均充分反应,实验数据如下:
(1)上述实验中发生反应的化学方程式为Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;
(2)根据固体的质量列出求解第二次实验消耗硫酸质量(x)的比例式$\frac{160}{294}$=$\frac{3.2g}{x}$;
(3)用98%的浓硫酸配制200g上述稀硫酸,需要加入水的质量是180g;
(4)若在恰好完全反应时停止加入稀硫酸,过滤,向所得的不饱和滤液中加入42g水,则最终所得的溶液中溶质的质量分数是10.15%;
(5)用150t该矿石可制得含杂质4%的生铁的质量是87.5t.
0 168178 168186 168192 168196 168202 168204 168208 168214 168216 168222 168228 168232 168234 168238 168244 168246 168252 168256 168258 168262 168264 168268 168270 168272 168273 168274 168276 168277 168278 168280 168282 168286 168288 168292 168294 168298 168304 168306 168312 168316 168318 168322 168328 168334 168336 168342 168346 168348 168354 168358 168364 168372 211419
| 物质 | 第一次 | 第二次 | 第三次 |
| 加入稀硫酸质量(g) | 60.0 | 60.0 | 60.0 |
| 剩余固体的质量(g) | 6.8 | 3.6 | 2.0 |
(2)根据固体的质量列出求解第二次实验消耗硫酸质量(x)的比例式$\frac{160}{294}$=$\frac{3.2g}{x}$;
(3)用98%的浓硫酸配制200g上述稀硫酸,需要加入水的质量是180g;
(4)若在恰好完全反应时停止加入稀硫酸,过滤,向所得的不饱和滤液中加入42g水,则最终所得的溶液中溶质的质量分数是10.15%;
(5)用150t该矿石可制得含杂质4%的生铁的质量是87.5t.
 A、B、C、D分别表示氧化物、单质、酸、盐四类物质中的一种,其中A在空气中燃烧时发出耀眼的白光,人体胃液中含有B物质,C是含银元素的盐,请回答下列问题:
A、B、C、D分别表示氧化物、单质、酸、盐四类物质中的一种,其中A在空气中燃烧时发出耀眼的白光,人体胃液中含有B物质,C是含银元素的盐,请回答下列问题:
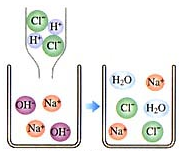 如图为某化学反应的微观模拟图,根据模拟图回答:
如图为某化学反应的微观模拟图,根据模拟图回答: 2014年10月24日前后哈尔滨市遭遇了几天雾霾天气,这样的天气给人们的出行带来了极大的不便,据调查哈市冬季供暖用煤为燃料是造成雾霾天气的成因之一.请回答相关问题:
2014年10月24日前后哈尔滨市遭遇了几天雾霾天气,这样的天气给人们的出行带来了极大的不便,据调查哈市冬季供暖用煤为燃料是造成雾霾天气的成因之一.请回答相关问题: 根据下列图片及文字回答问题:
根据下列图片及文字回答问题: