18.煤气(主要成分是CO)泄露会发生危险,因此常加入少量有特殊气味的乙硫醇(化学式为C2H5SH).乙硫醇燃烧的化学方程式为2C2H5SH+9X$\frac{\underline{\;点燃\;}}{\;}$4CO2+6H2O+2SO2.下列说法中正确的是( )
| A. | X的化学式为CO | B. | CO不仅能做燃料还可用于冶炼金属 | ||
| C. | CO2、SO2都是污染空气的有毒气体 | D. | 可以在室内放一盆水防止煤气中毒 |
17.生产加碘盐通常是在氯化钠中加入碘酸钾(KIO3).已知 KIO3中,K元素化合价为+1价,则I元素的化合价为( )
| A. | -l | B. | +l | C. | +5 | D. | +7 |
16.生活离不开化学.下列做法中,合理的是( )
| A. | 青少年适量补充微量元素铁以预防佝偻病 | |
| B. | 为了节约粮食,把霉变大米淘净后继续食用 | |
| C. | 利用硝酸铵溶于水吸热的原理,自制冰袋给发烧病人降温 | |
| D. | 食用甲醛浸泡的海产品,可提高人体免疫力 |
15.2010年的世界环境日是“减少污染--行动起来“.下列认识中,不正确的是( )
| A. | 植树造林,严禁乱砍滥伐 | |
| B. | 在生产和生活中提倡使用节能技术和节能用具 | |
| C. | 开发新能源,禁止开采和使用化石燃料 | |
| D. | 提倡乘坐公交车、骑自行车或步行的方式出行 |
14.下列变化中,属于物理变化的是( )
| A. | 牛奶变酸 | B. | 煤气中毒 | C. | 钢铁生锈 | D. | 酒精挥发 |
13.按照体积计算空气中氧气约占21%,某化学兴趣小组的同学按照课本的实验装置做“测定空气中氧气的体积分数”实验(图1),但测出的氧气体积分数明显偏小.请你参与探究:
【提出问题】
造成误差的原因是什么?如何改进课本实验装置?
【查阅资料】
①
②二氧化碳气体能被氢氧化钠溶液吸收
③在加热的条件下铜粉能与氧气反应生成黑色的氧化铜固体
【猜想】
甲同学:可能是导管内原存有空气,后来留有吸入的水,影响实验的准确性;
乙同学:可能是瓶内残留气体中还有氧气的缘故;
你还能做的猜想是集气瓶未冷却至室温就打开了弹簧夹(写一点即可).
【交流与讨论】
(1)写出图1中集气瓶中发生反应的文字或符号表达式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(2)丙同学认为,用木炭代替红磷也能完成图1的实验,但事先要在集气瓶中放入一定量的氢氧化钠溶液;
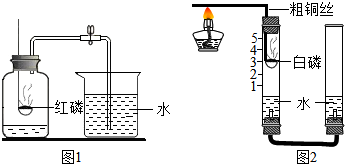
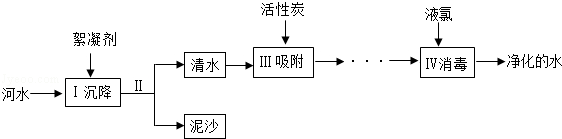
(3)他们对图1实验装置进行了如图2的改进.
①甲同学提出应把红磷更换为白磷,理由是白磷的着火点低,可以较容易的发生燃烧;
②通过粗铜丝来点燃玻璃管内的白磷,利用了金属铜的导热性;
③与图1实验装置相比,图2装置的一个优点是在密闭的环境中进行反应,能够减少实验误差;
【探究与反思】
(1)为验证乙同学的猜想,将铜粉在残余气体中加热,观察到铜粉变黑,所以乙同学的猜想合理(选填“合理”或“不合理”);
(2)大家采用改进的实验装置(图2)进行实验(左边玻璃管上面的空气平均分成了5等份,并标刻度线),待玻璃管冷却、管内白色的烟幕消失,同时能观察到左边玻璃管中水上升到1刻度线,得到了较准确的数据,但又意外发现左玻璃管内壁上端附着白色固体.左玻璃管上端的白色固体主要成分可能是白磷.
0 168051 168059 168065 168069 168075 168077 168081 168087 168089 168095 168101 168105 168107 168111 168117 168119 168125 168129 168131 168135 168137 168141 168143 168145 168146 168147 168149 168150 168151 168153 168155 168159 168161 168165 168167 168171 168177 168179 168185 168189 168191 168195 168201 168207 168209 168215 168219 168221 168227 168231 168237 168245 211419
【提出问题】
造成误差的原因是什么?如何改进课本实验装置?
【查阅资料】
①
| 颜色、状态 | 熔点/℃ | 燃烧所需最低温度/℃ | 密度/g•cm-3 | |
| 红磷 | 暗红色固体 | 590 | 240 | 2.34 |
| 白磷 | 白色固体 | 44.1 | 40 | 1.82 |
③在加热的条件下铜粉能与氧气反应生成黑色的氧化铜固体
【猜想】
甲同学:可能是导管内原存有空气,后来留有吸入的水,影响实验的准确性;
乙同学:可能是瓶内残留气体中还有氧气的缘故;
你还能做的猜想是集气瓶未冷却至室温就打开了弹簧夹(写一点即可).
【交流与讨论】
(1)写出图1中集气瓶中发生反应的文字或符号表达式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(2)丙同学认为,用木炭代替红磷也能完成图1的实验,但事先要在集气瓶中放入一定量的氢氧化钠溶液;

(3)他们对图1实验装置进行了如图2的改进.
①甲同学提出应把红磷更换为白磷,理由是白磷的着火点低,可以较容易的发生燃烧;
②通过粗铜丝来点燃玻璃管内的白磷,利用了金属铜的导热性;
③与图1实验装置相比,图2装置的一个优点是在密闭的环境中进行反应,能够减少实验误差;
【探究与反思】
(1)为验证乙同学的猜想,将铜粉在残余气体中加热,观察到铜粉变黑,所以乙同学的猜想合理(选填“合理”或“不合理”);
(2)大家采用改进的实验装置(图2)进行实验(左边玻璃管上面的空气平均分成了5等份,并标刻度线),待玻璃管冷却、管内白色的烟幕消失,同时能观察到左边玻璃管中水上升到1刻度线,得到了较准确的数据,但又意外发现左玻璃管内壁上端附着白色固体.左玻璃管上端的白色固体主要成分可能是白磷.
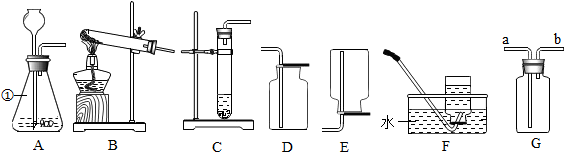
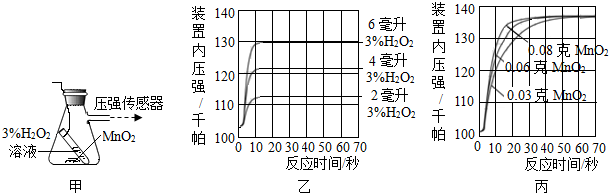
 (1)用正确的化学用语填空
(1)用正确的化学用语填空