7.下列有关物质溶解度的说法中,正确的是( )
| A. | 20℃时,10g某物质溶解在100g水中,故该物质20℃时的溶解度为$\frac{10g}{100g}$水 | |
| B. | 20℃时,把10g某物质溶解在水中制成饱和溶液,故20℃时,该物质的溶解度为$\frac{10g}{100g}$水 | |
| C. | 10g某物质溶解在100g水中达到饱和状态,这种物质的溶解度为$\frac{10g}{100g}$水 | |
| D. | 20℃时,10g某物质溶解在100g水中达到饱和状态,故该物质在20℃的溶解度为$\frac{10g}{100g}$水 |
5.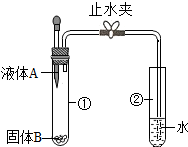 如图所示,打开止水夹,将液体A滴入试管①中,液体A与固体B接触,若在试管②中的导管口处没有气泡冒出,则下列液体A和固体B的组合可能是( )
如图所示,打开止水夹,将液体A滴入试管①中,液体A与固体B接触,若在试管②中的导管口处没有气泡冒出,则下列液体A和固体B的组合可能是( )
 如图所示,打开止水夹,将液体A滴入试管①中,液体A与固体B接触,若在试管②中的导管口处没有气泡冒出,则下列液体A和固体B的组合可能是( )
如图所示,打开止水夹,将液体A滴入试管①中,液体A与固体B接触,若在试管②中的导管口处没有气泡冒出,则下列液体A和固体B的组合可能是( )| A. | 水和氢氧化钠 | B. | 稀盐酸和铁 | C. | 水和生石灰 | D. | 水和硝酸铵 |
4.下列叙述与质量守恒定律相矛盾的是( )
①反应物的总质量等于生成物的总质量
②铁在氧气中燃烧后,生成物的质量大于铁的质量
③高锰酸钾加热分解后,剩余固体的质量比原高锰酸钾的质量减少了
④ag硫粉在bg氧气中点燃,生成二氧化硫的质量一定等于(a+b)g.
①反应物的总质量等于生成物的总质量
②铁在氧气中燃烧后,生成物的质量大于铁的质量
③高锰酸钾加热分解后,剩余固体的质量比原高锰酸钾的质量减少了
④ag硫粉在bg氧气中点燃,生成二氧化硫的质量一定等于(a+b)g.
| A. | ①④ | B. | ②③ | C. | ②③④ | D. | ④ |
3.工业制纯碱,是向饱和食盐水中通入氨气和二氧化碳,获得碳酸氢钠晶体,它的反应原理可用下列化学方程式表示:
NH3+CO2+H2O=NH4HCO3 …①
NH4HCO3+NaCl(饱和)=NaHCO3↓+NH4Cl …②
将所得碳酸氢钠晶体加热分解后即可得到纯碱.请回答:
(1)工业所制纯碱中常含有少量的氯化钠杂质,其原因是结晶析出的碳酸氢钠晶体表面沾有从溶液中带出的少量氯化钠.
(2)现有甲、乙两组的学生,欲测定某工业纯碱样品中Na2CO3的质量分数,分别设计并完成实验如下.
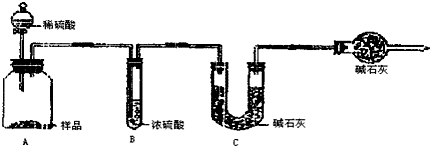
甲组:取10.00g样品,利用上图所示装置,测出反应后装置C中碱石灰的增重为3.3g.
乙组:取10.00g样品,向其中加入过量的盐酸,直至样品中无气泡冒出,加热蒸发所得物并在干燥器中冷却至室温后称量.反复加热、冷却、称量,直至所称量的固体质量几乎不变为止,此时所得固体的质量为10.99g.
请分析、计算后填表:
0 167124 167132 167138 167142 167148 167150 167154 167160 167162 167168 167174 167178 167180 167184 167190 167192 167198 167202 167204 167208 167210 167214 167216 167218 167219 167220 167222 167223 167224 167226 167228 167232 167234 167238 167240 167244 167250 167252 167258 167262 167264 167268 167274 167280 167282 167288 167292 167294 167300 167304 167310 167318 211419
NH3+CO2+H2O=NH4HCO3 …①
NH4HCO3+NaCl(饱和)=NaHCO3↓+NH4Cl …②
将所得碳酸氢钠晶体加热分解后即可得到纯碱.请回答:
(1)工业所制纯碱中常含有少量的氯化钠杂质,其原因是结晶析出的碳酸氢钠晶体表面沾有从溶液中带出的少量氯化钠.
(2)现有甲、乙两组的学生,欲测定某工业纯碱样品中Na2CO3的质量分数,分别设计并完成实验如下.

甲组:取10.00g样品,利用上图所示装置,测出反应后装置C中碱石灰的增重为3.3g.
乙组:取10.00g样品,向其中加入过量的盐酸,直至样品中无气泡冒出,加热蒸发所得物并在干燥器中冷却至室温后称量.反复加热、冷却、称量,直至所称量的固体质量几乎不变为止,此时所得固体的质量为10.99g.
请分析、计算后填表:
| 分析与计算 | 计算样品中碳酸钠的质量分数 | 对实验结果的评价 | 实验失败的主要原因及对结果的影响 |
| 甲组 | 79.5% | 失败 | 加入的稀硫酸没有完全将碳酸钠反应掉,且没有冷却至室温,部分二氧化碳存在于装置内,没有被C装置内的碱石灰所吸收,造成测量结果偏小 |
| 乙组 | 99.6% | 成功 |
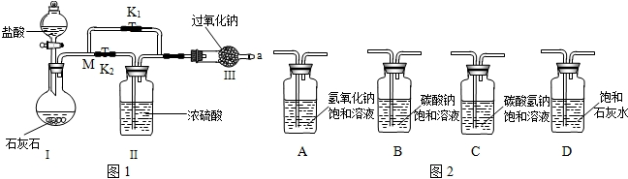

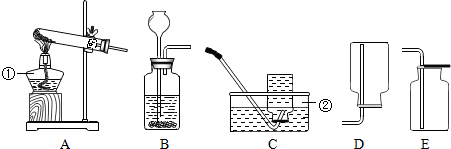
 我国蕴藏着丰富的海洋资源,而淡水资源短缺,需要合理利用,爱护水资源.
我国蕴藏着丰富的海洋资源,而淡水资源短缺,需要合理利用,爱护水资源.