9.下列各组物质中,仅用一种试剂不能鉴别的一组是( )
| A. | Cu粉 Fe粉 Fe2O3粉 | |
| B. | Na2CO3 BaCl2 KNO3 | |
| C. | NaCl固体 CuSO4固体 CaCO3固体 | |
| D. | (NH4)2SO4 KNO3 NaNO3 |
8.水是生命的源泉,下列“水”中属于纯净物的是( )
| A. | 矿泉水 | B. | 冰水混合物 | C. | 雨水 | D. | 自来水 |
6.某化学兴趣小组如图1模拟教材中的炼铁实验,再将所得的黑色粉末物质与足量的稀硫酸反应,发现黑色粉末消失,但始终没有气泡生成.
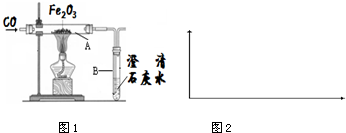
(1)铁元素的常见价态有+2、+3.将Fe3O4表示为两种氧化物的结合形式FeO•Fe2O3.
(2)根据现象“没有气泡生成”猜想,黑色粉末物质可能是:
①氧化亚铁;②四氧化三铁;③氧化亚铁和四氧化三铁的混合物.
(3)图中装置有明显缺陷,从环保角度出发,应采取的措施是将尾气点燃.
(4)从实验安全角度考虑,应在装置A、B间增加一个安全瓶,可以有效防止B中的澄清石灰水倒吸入A中.
(5)某科技小组查阅CO与Fe2O3反应各产物开始生成的温度情况:
Fe2O3$\stackrel{300℃以上}{→}$Fe3O4$\stackrel{600℃以上}{→}$FeO$\stackrel{700℃以上}{→}$Fe
由于酒精灯通常只能提供400-500℃的温度,则黑色粉末的成分理论上可确定为Fe3O4.
(6)设计实验对黑色粉末进行探究.
某同学选用X溶液与黑色粉末反应,也可以证明黑色粉末中不含有Fe,则X为A.
A.硫酸铜溶液 B.硫酸钠溶液 C.氢氧化钠溶液 D.氢氧化钙溶液
(7)在一定温度下,该科研小组将3.2克Fe2O3与足量的CO混合加热,反应结束后冷却,精确称量黑色粉末质量为ag(计算保留两位有效数字)
①若a=2.24g,黑色粉末是Fe;②若a=2.88g,黑色粉末是FeO;③若a=3.09g,黑色粉末是Fe3O4;
④若黑色粉末是混合物则a的取值范围是2.24g<a<3.09g.
(8)请你画出以温度为横坐标,玻璃管中剩余固体的质量为纵坐标(如图2),表示用CO还原Fe2O3.

(1)铁元素的常见价态有+2、+3.将Fe3O4表示为两种氧化物的结合形式FeO•Fe2O3.
(2)根据现象“没有气泡生成”猜想,黑色粉末物质可能是:
①氧化亚铁;②四氧化三铁;③氧化亚铁和四氧化三铁的混合物.
(3)图中装置有明显缺陷,从环保角度出发,应采取的措施是将尾气点燃.
(4)从实验安全角度考虑,应在装置A、B间增加一个安全瓶,可以有效防止B中的澄清石灰水倒吸入A中.
(5)某科技小组查阅CO与Fe2O3反应各产物开始生成的温度情况:
Fe2O3$\stackrel{300℃以上}{→}$Fe3O4$\stackrel{600℃以上}{→}$FeO$\stackrel{700℃以上}{→}$Fe
由于酒精灯通常只能提供400-500℃的温度,则黑色粉末的成分理论上可确定为Fe3O4.
(6)设计实验对黑色粉末进行探究.
| 操作步骤 | 实验现象 | 解释或反应方程式 |
| 1.取少量黑色物质加入 30%热的盐酸中 | 无气泡、溶液颜 色变成黄绿色 | 该反应的化学方程式:Fe3O4+8HCl═FeCl2+2FeCl3+4H2O |
| 2.用磁铁吸引此粉末 | 能够被吸引 | 说明该物质具有磁性 |
A.硫酸铜溶液 B.硫酸钠溶液 C.氢氧化钠溶液 D.氢氧化钙溶液
(7)在一定温度下,该科研小组将3.2克Fe2O3与足量的CO混合加热,反应结束后冷却,精确称量黑色粉末质量为ag(计算保留两位有效数字)
①若a=2.24g,黑色粉末是Fe;②若a=2.88g,黑色粉末是FeO;③若a=3.09g,黑色粉末是Fe3O4;
④若黑色粉末是混合物则a的取值范围是2.24g<a<3.09g.
(8)请你画出以温度为横坐标,玻璃管中剩余固体的质量为纵坐标(如图2),表示用CO还原Fe2O3.
5. 小明记得在学习金属活动性顺序的应用时,老师曾说过一般不会用K、Ca、Na等活泼金属和盐溶液进行置换反应,因为这些金属能直接和水发生反应生成对应的碱和氢气.小明查阅资料如下:
小明记得在学习金属活动性顺序的应用时,老师曾说过一般不会用K、Ca、Na等活泼金属和盐溶液进行置换反应,因为这些金属能直接和水发生反应生成对应的碱和氢气.小明查阅资料如下:
【资料卡片】:
(1)Na和冷水剧烈反应,2Na+2H2O═2NaOH+H2↑;
(2)镁和冷水反应缓慢,和沸水反应剧烈,Mg+2H2O═Mg(OH)2+H2↑;
(3)Al和沸水反应非常缓慢,2Al+6H2O═2Al(OH)3+3H2↑;
Ⅰ、从上述资料中,你能得出金属和水反应的条件和产物有何不同和相似之处?
(1)相同点:都生成碱和氢气;
(2)不同点:反应的剧烈程度不同.
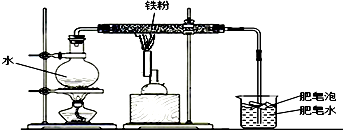
Ⅱ、小明对此非常好奇,在老师的帮助下,查阅了相关资料并做了铁粉在高温条件下和水蒸气的反应,装置如下图所示:
【资料卡片】:
A、铁的氧化物的热稳定性顺序是FeO(黑色)>Fe3O4>Fe2O3,且Fe3O4有磁性;
B、Fe2O3分解温度在1400℃以上,Fe3O4分解温度在1538℃以上;
C、Fe(OH)2是一种白色固体,在空气很快变成灰绿色,最终变为红褐色.
实验进行2分钟后,用燃着的木条点燃肥皂泡,可以观察到一团火焰.同时发现玻璃管内灰黑色物质先红热,最终变成黑色晶体,整个实验持续10分钟左右.
(1)你认为该反应为什么要在高温下才能进行?保证了四氧化三铁、氧化铁的分解;
(2)火焰的产生,说明该反应生成了氢气,在点燃该气体前,一定要检验纯度;
(3)实验结束后,所进行的实验操作应该是先撤导管,后熄灭酒精灯.这样做的目的是防止水槽中水倒流,炸裂试管.
Ⅲ、通过Ⅱ中的实验现象,大家对反应后玻璃管中残留的黑色物质的成分猜想如下:
1:Fe(OH)3;2:Fe(OH)2;3:FeO;4:Fe2O3;5:Fe3O4;6:Fe.(可多填)
甲同学认为:猜想1、2、4明显错误,理由是氢氧化铁、氢氧化亚铁、氧化铁热稳定性差;
对于其他猜想,同学们又做了如下实验:
甲同学根据实验现象,认为此黑色物质是Fe3O4,但对于他的结论,乙同学认为不妥,他的理由是铁也能被磁铁吸引;
根据甲、乙两同学的实验,还可以排除猜想3、5,理由是氧化亚铁、四氧化三铁不会与稀盐酸反应生成气体;
为进一步确认此黑色物质,同学们再次进行了实验:
结合资料综合分析,回答下列问题:
(1)玻璃管中残留的黑色物质应为碳,铁粉和水蒸气在高温下反应的化学方程式为:3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,属于置换反应;
(2)实验1中的A溶液为硫酸铜溶液,加A溶液的目的是验证黑色物质中含有铁.
Ⅳ、丙同学用定量的方法确定实验后玻璃管中黑色物质的组成.方案如下:
将5.6gFe粉和足量的H2O(气)充分反应后,得到7.2g黑色固体,再将此黑色固体加入150g足量稀盐酸中继续反应,充分反应后,称得烧杯内溶液质量为157.15g.请根据上述数据计算出7.2g黑色物质的组成,确证上述探究结论.(写出计算过程)
Ⅴ、反思评价:
(1)该氧化物又可以经过此反应的逆反应生成颗粒很细的铁粉.这种铁粉具有很高的反应活性,在空气中受撞击或加热时会燃烧,所以俗称“引火铁”.写出此反应的化学方程式:
Fe3O4+4H2$\frac{\underline{\;高温\;}}{\;}$3Fe+4H2O;
(2)砖窑用粘土烧制青砖(颜色发黑的砖)时,窑内温度可达1150℃,Fe2O3和H2反应生成FeO,写出该反应的化学方程式Fe2O3+H2$\frac{\underline{\;1150℃\;}}{\;}$2FeO+H2O.
 小明记得在学习金属活动性顺序的应用时,老师曾说过一般不会用K、Ca、Na等活泼金属和盐溶液进行置换反应,因为这些金属能直接和水发生反应生成对应的碱和氢气.小明查阅资料如下:
小明记得在学习金属活动性顺序的应用时,老师曾说过一般不会用K、Ca、Na等活泼金属和盐溶液进行置换反应,因为这些金属能直接和水发生反应生成对应的碱和氢气.小明查阅资料如下:【资料卡片】:
(1)Na和冷水剧烈反应,2Na+2H2O═2NaOH+H2↑;
(2)镁和冷水反应缓慢,和沸水反应剧烈,Mg+2H2O═Mg(OH)2+H2↑;
(3)Al和沸水反应非常缓慢,2Al+6H2O═2Al(OH)3+3H2↑;
Ⅰ、从上述资料中,你能得出金属和水反应的条件和产物有何不同和相似之处?
(1)相同点:都生成碱和氢气;
(2)不同点:反应的剧烈程度不同.
Ⅱ、小明对此非常好奇,在老师的帮助下,查阅了相关资料并做了铁粉在高温条件下和水蒸气的反应,装置如下图所示:
【资料卡片】:
A、铁的氧化物的热稳定性顺序是FeO(黑色)>Fe3O4>Fe2O3,且Fe3O4有磁性;
B、Fe2O3分解温度在1400℃以上,Fe3O4分解温度在1538℃以上;
C、Fe(OH)2是一种白色固体,在空气很快变成灰绿色,最终变为红褐色.
实验进行2分钟后,用燃着的木条点燃肥皂泡,可以观察到一团火焰.同时发现玻璃管内灰黑色物质先红热,最终变成黑色晶体,整个实验持续10分钟左右.
(1)你认为该反应为什么要在高温下才能进行?保证了四氧化三铁、氧化铁的分解;
(2)火焰的产生,说明该反应生成了氢气,在点燃该气体前,一定要检验纯度;
(3)实验结束后,所进行的实验操作应该是先撤导管,后熄灭酒精灯.这样做的目的是防止水槽中水倒流,炸裂试管.
Ⅲ、通过Ⅱ中的实验现象,大家对反应后玻璃管中残留的黑色物质的成分猜想如下:
1:Fe(OH)3;2:Fe(OH)2;3:FeO;4:Fe2O3;5:Fe3O4;6:Fe.(可多填)
甲同学认为:猜想1、2、4明显错误,理由是氢氧化铁、氢氧化亚铁、氧化铁热稳定性差;
对于其他猜想,同学们又做了如下实验:
| 实验方案 | 实验现象 | |
| 甲 | 将磁铁靠近黑色粉末 | 黑色粉末可被磁铁全部吸引 |
| 乙 | 取少量黑色粉末加入稀盐酸中 | 有气泡 |
根据甲、乙两同学的实验,还可以排除猜想3、5,理由是氧化亚铁、四氧化三铁不会与稀盐酸反应生成气体;
为进一步确认此黑色物质,同学们再次进行了实验:
| 实验方案 | 实验现象 | 结论或化学方程式 |
| 1、取实验后的黑色粉末,加入足量的A溶液,搅拌使反应充分. | 黑色物质表面有红色物质,溶液颜色出现较浅的绿色,烧杯底部仍有较多黑色物质 | Fe+CuSO4=FeSO4+Cu |
| 2、过滤、洗涤、干燥,再用磁铁吸引 | 黑色物质可被磁铁全部吸引,留下红色固体 | 被磁铁吸引的物质是铁 |
(1)玻璃管中残留的黑色物质应为碳,铁粉和水蒸气在高温下反应的化学方程式为:3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,属于置换反应;
(2)实验1中的A溶液为硫酸铜溶液,加A溶液的目的是验证黑色物质中含有铁.
Ⅳ、丙同学用定量的方法确定实验后玻璃管中黑色物质的组成.方案如下:
将5.6gFe粉和足量的H2O(气)充分反应后,得到7.2g黑色固体,再将此黑色固体加入150g足量稀盐酸中继续反应,充分反应后,称得烧杯内溶液质量为157.15g.请根据上述数据计算出7.2g黑色物质的组成,确证上述探究结论.(写出计算过程)
Ⅴ、反思评价:
(1)该氧化物又可以经过此反应的逆反应生成颗粒很细的铁粉.这种铁粉具有很高的反应活性,在空气中受撞击或加热时会燃烧,所以俗称“引火铁”.写出此反应的化学方程式:
Fe3O4+4H2$\frac{\underline{\;高温\;}}{\;}$3Fe+4H2O;
(2)砖窑用粘土烧制青砖(颜色发黑的砖)时,窑内温度可达1150℃,Fe2O3和H2反应生成FeO,写出该反应的化学方程式Fe2O3+H2$\frac{\underline{\;1150℃\;}}{\;}$2FeO+H2O.
4.在天平的两边放有两只烧杯,再向两只烧杯内分别加入100克9.8%的稀硫酸,向左边和右边分别加入等质量的铁和镁充分反应后天平依旧保持平衡,则加入的铁和镁的质量可能为( )
| A. | 2g | B. | 2.4g | C. | 5.6g | D. | 10g |
2.体操运动员在完成单杠、吊环项目时常用“镁粉”搓手,以起到防滑效果.某种“镁粉”中可能含有Mg、MgO、Mg(OH)2、MgCO3中的一种或两种固体,实验小组对其成分展开了探究.
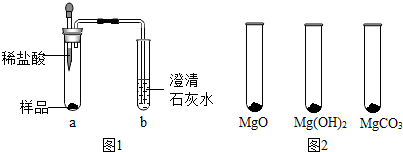
已知:MgO+2HCl═MgCl2+H2O MgCO3+2HCl═MgCl2+H2O+CO2↑
(1)探究“镁粉”中是否含有Mg和MgCO3
①取少量样品,如图1所示进行实验.观察到a试管中有气泡产生,b试管中产生的现象是澄清的石灰水变浑浊.则证明“镁粉”中一定含有MgCO3.
②为证明“镁粉”中是否含有Mg,小明将燃着的木条放在图中b试管口上方,木条熄灭.但同学们指出,该实验不能达成实验目的,需要将图中的澄清石灰水替换成氢氧化钠浓溶液.小明按照修改后的实验方案重复上述实验,观察到b试管口无明显现象,证明“镁粉”中不含Mg.
(2)探究“镁粉”中是否还含有MgO及Mg(OH)2
【实验过程】
Ⅰ.用MgO、Mg(OH)2和MgCO3三种固体分别做性质实验.分别取0.5g三种固体粉末,每次取样方法如图2所示:
逐滴加入相同溶质质量分数的稀盐酸直至粉末恰好消失.在下表中记录消耗的同浓度稀盐酸的体积(以下体积均在同一条件下测定,且保留到小数点后1位)
Ⅱ.取“镁粉”样品0.5g,加入上述稀盐酸至粉末恰好溶解.此时消耗稀盐酸的体积约为5.3mL.
【实验分析及结论】“镁粉”不只含有MgCO3.理由是0.5gMgCO3消耗的盐酸体积与0.5g“镁粉”消耗的盐酸体积不相等.
【实验反思】为确定“镁粉”的具体成分,同学们认为还需要补充如下实验:分别取0.5g“镁粉”和0.5gMgCO3,加入足量稀盐酸,测定生成的气体体积分别为119mL和140mL.由此可知“镁粉”中含有MgCO3的质量分数为85%,“镁粉”中除MgCO3外的另一种物质为Mg(OH)2.
0 166128 166136 166142 166146 166152 166154 166158 166164 166166 166172 166178 166182 166184 166188 166194 166196 166202 166206 166208 166212 166214 166218 166220 166222 166223 166224 166226 166227 166228 166230 166232 166236 166238 166242 166244 166248 166254 166256 166262 166266 166268 166272 166278 166284 166286 166292 166296 166298 166304 166308 166314 166322 211419

已知:MgO+2HCl═MgCl2+H2O MgCO3+2HCl═MgCl2+H2O+CO2↑
(1)探究“镁粉”中是否含有Mg和MgCO3
①取少量样品,如图1所示进行实验.观察到a试管中有气泡产生,b试管中产生的现象是澄清的石灰水变浑浊.则证明“镁粉”中一定含有MgCO3.
②为证明“镁粉”中是否含有Mg,小明将燃着的木条放在图中b试管口上方,木条熄灭.但同学们指出,该实验不能达成实验目的,需要将图中的澄清石灰水替换成氢氧化钠浓溶液.小明按照修改后的实验方案重复上述实验,观察到b试管口无明显现象,证明“镁粉”中不含Mg.
(2)探究“镁粉”中是否还含有MgO及Mg(OH)2
【实验过程】
Ⅰ.用MgO、Mg(OH)2和MgCO3三种固体分别做性质实验.分别取0.5g三种固体粉末,每次取样方法如图2所示:
逐滴加入相同溶质质量分数的稀盐酸直至粉末恰好消失.在下表中记录消耗的同浓度稀盐酸的体积(以下体积均在同一条件下测定,且保留到小数点后1位)
| MgO | Mg(OH)2 | MgCO3 | |
| 消耗稀盐酸的体积/mL | 10.4 | 7.2 | 5.0 |
【实验分析及结论】“镁粉”不只含有MgCO3.理由是0.5gMgCO3消耗的盐酸体积与0.5g“镁粉”消耗的盐酸体积不相等.
【实验反思】为确定“镁粉”的具体成分,同学们认为还需要补充如下实验:分别取0.5g“镁粉”和0.5gMgCO3,加入足量稀盐酸,测定生成的气体体积分别为119mL和140mL.由此可知“镁粉”中含有MgCO3的质量分数为85%,“镁粉”中除MgCO3外的另一种物质为Mg(OH)2.
 某化学兴趣小组利用如图所示装置探究两个实验.
某化学兴趣小组利用如图所示装置探究两个实验. 实验室中用如下实验来研究铁、铝、铜三种金属活动顺序及其在活动顺序表中相对氢的位置.
实验室中用如下实验来研究铁、铝、铜三种金属活动顺序及其在活动顺序表中相对氢的位置.